2015-2016学年黑龙江省齐齐哈尔市九年级上学期期中化学试卷(五四学制)
试卷日期:2016-12-21 考试类型:期中考试
一、选择题
-
1. 地壳中含量最多的金属元素是( )A、氧 B、硅 C、铁 D、铝2. 下列物质与水混合,不能形成溶液的是( )A、食盐 B、二氧化碳 C、植物油 D、酒精3. 溶液对人类的生产、生活都有很重要的意义.下列关于溶液的说法正确的是( )A、均一、稳定的液体都是溶液 B、溶液组成中一定含有水 C、饱和溶液就是不能再溶解任何物质的溶液 D、融雪剂的作用原理是利用某些物质水溶液的凝固点低于0℃4. 在配制硝酸钾溶液的过程中,下列操作不能加快硝酸钾溶解速率的是( )A、将水的温度从20℃升高到60℃ B、增大压强 C、在加入硝酸钾的同时不断搅拌 D、将硝酸钾固体研磨成粉末5. 下列不能作为判断金属Mg、Fe、Cu三种金属活动性强弱的是的是( )A、在纯氧中燃烧的现象 B、与盐酸反应的快慢程度 C、金属导电性强弱 D、三种金属发现和利用的年代的先后顺序6. 将一枚洁净的铁钉浸入稀硫酸中,下列叙述正确的是( )
①铁钉表面产生气泡;
②液体由无色逐渐变为浅绿色;
③铁钉的质量减轻;
④液体的质量减轻.
A、②③ B、①②④ C、①②③ D、①②③④7. 下列关于反应的描述,反应方程式及反应类型完全正确的是( )A、实验室用加热高锰酸钾制取氧气2KMnO4 K2MnO4+MnO2+O2↑ 分解反应 B、铁丝在氧气中燃烧 4Fe+3O2 2Fe2O3化合反应 C、高炉炼铁原理 Fe2O3+3CO 2Fe+3CO2 复分解反应 D、将铁片投入足量的稀盐酸中2Fe+6HCl═2FeCl3+3H2↑ 置换反应8. 20℃时,向100g未知浓度KCl溶液中加入5g KCl后,正确的是( )A、溶液质量变为105g B、溶剂质量不变 C、溶液浓度一定变大 D、溶质质量一定发生变化9.将等质量的甲、乙两金属分别与足量的稀硫酸反应,产生氢气的质量与反应时间的关系如图.关于甲、乙两金属判断合理的是( )
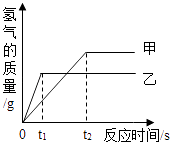 A、铁、镁 B、铁、锌 C、锌、铁 D、锌、镁10. 向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤,不可能存在的情况是( )A、滤纸上有Ag,滤液中有Cu2+、Ag+ B、滤纸上有Ag,滤液中有Fe2+、Cu2+ C、滤纸上有Ag、Cu,滤液中有Fe2+、Cu2+ D、滤纸上有Ag、Cu,滤液中有Fe2+
A、铁、镁 B、铁、锌 C、锌、铁 D、锌、镁10. 向AgNO3、Cu(NO3)2的混合溶液中加入一些铁粉,完全反应后过滤,不可能存在的情况是( )A、滤纸上有Ag,滤液中有Cu2+、Ag+ B、滤纸上有Ag,滤液中有Fe2+、Cu2+ C、滤纸上有Ag、Cu,滤液中有Fe2+、Cu2+ D、滤纸上有Ag、Cu,滤液中有Fe2+二、填空题
-
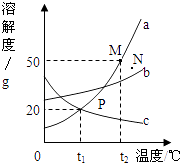
11. 金属与人类的生活和生产密切相关(1)、铝、铁、铜是人类广泛使用的三种金属,人类大规模开发利用这三种金属的先后排列顺序是 (用元素符号表示);(2)、铝比铁活泼,但铝制品却比铁制品耐腐蚀的原因是 .(3)、一般情况下,若跟组成它的成分相比,合金的硬度 , 熔点;(填“增大”或“降低”)(4)、西汉时期,我国劳动人民就会运用湿法冶金制铜,这种制铜方法的化学方程式是;氢气还原氧化铜也可以得到铜,发生反应的化学方程式为 .12. 下图是a、b、c三种物质的溶解度曲线,根据图象回答下列问题:
 (1)、P点的含义是 .(2)、t2℃时30ga物质加入到50g水中不断搅拌,能形成 g溶液.(3)、t2℃时a、b、c三种物质的溶解度按由大到小的顺序排列是(填写物质序号).(4)、相同质量的a、b、c三种物质t2℃时的饱和溶液降温到t1℃时,析出晶体较多的是 , 没有晶体析出的是 .(5)、将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大到小关系是(填写物质序号).(6)、M,N两点均表示a物质的溶液,下列做法不能实现M,N间的相互转化的是A、从N→M:先向N中加入适量的固体a再降温 B、从N→M:先将N降温再加入适量固体a C、从M→N:先将M降温再将其升温 D、从M→N:先将M升温再将其蒸发掉部分水.13. 在花卉市场上经常见到用营养液培育观赏植物.配制营养液的主要试剂之一是质量分数为1.4%的KNO3溶液,现欲配制这种KNO3溶液200克.(1)、需KNO3固体克.(2)、配制此KNO3溶液的步骤为:a.计算 b.称量(量取)c.溶解 d.装入试剂瓶.仪器(1)托盘天平(2)烧杯(3)量筒(4)教头滴管(5)蒸发皿.在以上给出的仪器中,有一个仪器在配制溶液过程中不需要的是 , 同时,若要成功配制此溶液,还缺少一个重要的仪器是 , 此仪器在配制过程中所起的作用是 .(3)、下列方法能使接近饱和KNO3溶液由不饱和变为饱和的是 . (从①﹣﹣⑥中选序号填入)
(1)、P点的含义是 .(2)、t2℃时30ga物质加入到50g水中不断搅拌,能形成 g溶液.(3)、t2℃时a、b、c三种物质的溶解度按由大到小的顺序排列是(填写物质序号).(4)、相同质量的a、b、c三种物质t2℃时的饱和溶液降温到t1℃时,析出晶体较多的是 , 没有晶体析出的是 .(5)、将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大到小关系是(填写物质序号).(6)、M,N两点均表示a物质的溶液,下列做法不能实现M,N间的相互转化的是A、从N→M:先向N中加入适量的固体a再降温 B、从N→M:先将N降温再加入适量固体a C、从M→N:先将M降温再将其升温 D、从M→N:先将M升温再将其蒸发掉部分水.13. 在花卉市场上经常见到用营养液培育观赏植物.配制营养液的主要试剂之一是质量分数为1.4%的KNO3溶液,现欲配制这种KNO3溶液200克.(1)、需KNO3固体克.(2)、配制此KNO3溶液的步骤为:a.计算 b.称量(量取)c.溶解 d.装入试剂瓶.仪器(1)托盘天平(2)烧杯(3)量筒(4)教头滴管(5)蒸发皿.在以上给出的仪器中,有一个仪器在配制溶液过程中不需要的是 , 同时,若要成功配制此溶液,还缺少一个重要的仪器是 , 此仪器在配制过程中所起的作用是 .(3)、下列方法能使接近饱和KNO3溶液由不饱和变为饱和的是 . (从①﹣﹣⑥中选序号填入)①加水 ②加KNO3固体 ③蒸发水 ④冷却 ⑤加热但保持溶液质量不变 ⑥加饱和KNO3溶液
(4)、现向KNO3饱和溶液中,逐滴加水稀释使其质量分数降至1.4%,在此稀释过程中,符合此溶液中溶质质量变化规律的图示是 .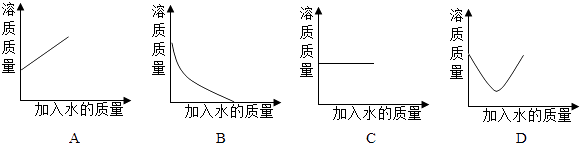 14. 化学实验室要从X,银、铜、锌四种金属混合物中分离某贵重金属.流程如下:
14. 化学实验室要从X,银、铜、锌四种金属混合物中分离某贵重金属.流程如下: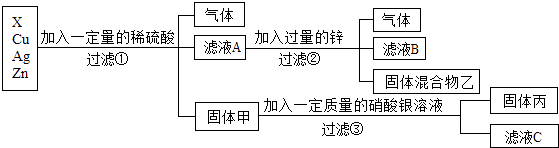
请回答:
(1)、四种金属的活动性顺序由强到弱的是;(2)、固体丙中一定含有的金属是;(3)、写出③中反应的化学方程式;(4)、为了检验滤液C中的溶质成分:向其中加入稀盐酸,有白色沉淀产生,则滤液C中一定含有的阳离子 .三、实验题
-
15. 在研究“铁生锈的条件”的实验中,某兴趣小组对实验进行了创新设计,请把实验报告补充完整.(1)、【实验目的】铁生锈条件的探究.
【实验内容】取3段光亮无锈的细铁丝,绕成螺旋状,放入3支干燥洁净的试管底部,进行下列实验,实验要保证有足够长的时间来观察现象.
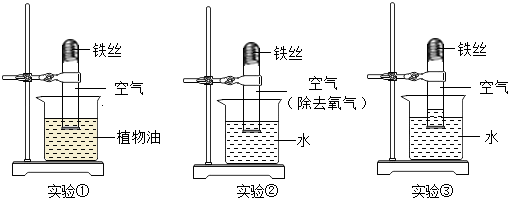
【实验现象】实验①②无明显现象,实验③中铁丝 , 且试管内水面 .
(2)、【实验结论】铁生锈实际上是铁与空气中的发生反应的结果.(3)、【实验思考】①当铁丝足量,时间足够长,实验③进入试管内的水的体积约占试管体积的 .
②该实验创新之处在于可根据铁丝表面的铁锈和两种现象来判断铁丝反应进行的情况.
③防止菜刀生锈的方法有 . (写一种)
16. 小红发现,金店里有两种不同的“白金”,单价相差悬殊,小红很好奇,打算进行研究.【查阅资料】市场上所谓的“白金”通常有两种,一种是金、镍、铜、锌的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,用于耐腐蚀的化学仪器及首饰等,俗称“白金”[platinum]﹣﹣﹣﹣﹣﹣元素符号Pt.小红结合化学课上学习的金属活动性顺序,展开了下列实验活动.
(1)、鉴别两种白金,她的方法可能是;(2)、探究Zn、Ni(镍)、铜的活动性顺序.【做出假设】对三种金属的活动性顺序提出可能的假设①Zn>Ni>Cu;②Zn>Cu>Ni你觉得还有其他的可能性吗?请把它们写出来(一种即可)
假设:③
(3)、【查阅资料】小红同学查阅了部分含镍化合物的溶解性如下表,且得知镍能与酸反应.OH﹣
NO3﹣
SO42﹣
Cl﹣
Ni2+
不
溶
溶
溶
【设计实验】同温下,取大小、厚度相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象.
【记录现象】请帮助小红把实验现象填写完整
金属
Ni
Zn
Cu
与盐酸反应的现象
气体产生缓慢
金属逐渐溶解
气体产生激烈
金属迅速溶解
(4)、【得出结论】原假设中正确的是(填序号)写出镍与盐酸反应的化学方程式 .
(5)、【结论应用】①根据探究结果,请你预测镍与硫酸铜溶液(填“能”或“不能”)反应,理由是 .
②除小红的实验设计外,你能否像小红一样,设计另一组实验,也这样一次验证上述假设的正确与否,你的设计所用的一组物质的化学式是(只写出一组即可).
四、计算题
-
17. 13g锌投入到200g硫酸溶液中,恰好完全反应.求:(1)、该硫酸溶液的溶质质量分数?(2)、反应后所得溶液的溶质质量分数?