广东省茂名高州市东岸中学2016-2017学年九年级化学一模考试试卷
试卷日期:2018-02-28 考试类型:中考模拟
一、单选题
-
1. 生产、生活中的下列变化,属于物理变化的是( )
A、钢铁生锈 B、粮食酿酒 C、石油分馏 D、木炭燃烧2. 通过实验测定了空气的组成的科学家是( )
A、门捷列夫 B、达尔文
B、达尔文  C、牛顿
C、牛顿  D、拉瓦锡
D、拉瓦锡  3. 下列安全图标中,表示“禁止燃放鞭炮”的是( )A、
3. 下列安全图标中,表示“禁止燃放鞭炮”的是( )A、
B、
B、
C、
C、
D、
D、
4. 下列符号中,表示2个氯原子的是( )A、2Cl B、2Cl2 C、Cl2 D、2Cl-5. 下列事实中,属于物质化学性质的是( )A、普通玻璃属于易碎品 B、二氧化碳能使澄清石灰水变浑浊 C、金刚石硬度大 D、盛有水和植物油的试管振荡得到乳状浑浊液体6. 下列物质属于混合物的是( )A、水银 B、液氮 C、干冰 D、生铁7. 如图是某原子的结构示意图。下列关于该原子的说法不正确的是( )
4. 下列符号中,表示2个氯原子的是( )A、2Cl B、2Cl2 C、Cl2 D、2Cl-5. 下列事实中,属于物质化学性质的是( )A、普通玻璃属于易碎品 B、二氧化碳能使澄清石灰水变浑浊 C、金刚石硬度大 D、盛有水和植物油的试管振荡得到乳状浑浊液体6. 下列物质属于混合物的是( )A、水银 B、液氮 C、干冰 D、生铁7. 如图是某原子的结构示意图。下列关于该原子的说法不正确的是( ) A、属于金属元素原子 B、最外层电子数为 7 C、容易得到电子 D、有 3 个电子层8. 将铜丝插入下列溶液中,有明显现象的是( )A、HCl溶液 B、AgNO3溶液 C、MgSO4溶液 D、Ba(OH)2溶液9. Sb2O5 是一种重要的阻燃剂,工业制取该物质的化学方程式为:Sb2O3 + 2X = Sb2O5 + 2H2O.则 X 的化学式为( )A、H2 B、O2 C、H2O2 D、H3SbO410. 下列关于水的说法正确的是( )A、水资源可以循环利用,没必要担心淡水资源不足 B、蒸馏水中加入肥皂水,振荡后有较多泡沫产生 C、矿泉水是纯净物 D、硬水通过活性炭吸附后可变成软水11. 乙硫醇(化学式为C2H6S)易挥发,有蒜臭味,人对该气味极其敏感,下列有关乙硫醇的说法不正确的是 ( )A、乙硫醇的相对分子质量为52 B、乙硫醇中C,H,S三种元素的原子个数比是2:6:1 C、硫元素的质量分数是 ×100% D、在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏12. 下列实验操作符合规范的是( )A、塞紧橡胶塞
A、属于金属元素原子 B、最外层电子数为 7 C、容易得到电子 D、有 3 个电子层8. 将铜丝插入下列溶液中,有明显现象的是( )A、HCl溶液 B、AgNO3溶液 C、MgSO4溶液 D、Ba(OH)2溶液9. Sb2O5 是一种重要的阻燃剂,工业制取该物质的化学方程式为:Sb2O3 + 2X = Sb2O5 + 2H2O.则 X 的化学式为( )A、H2 B、O2 C、H2O2 D、H3SbO410. 下列关于水的说法正确的是( )A、水资源可以循环利用,没必要担心淡水资源不足 B、蒸馏水中加入肥皂水,振荡后有较多泡沫产生 C、矿泉水是纯净物 D、硬水通过活性炭吸附后可变成软水11. 乙硫醇(化学式为C2H6S)易挥发,有蒜臭味,人对该气味极其敏感,下列有关乙硫醇的说法不正确的是 ( )A、乙硫醇的相对分子质量为52 B、乙硫醇中C,H,S三种元素的原子个数比是2:6:1 C、硫元素的质量分数是 ×100% D、在管道煤气中添加微量乙硫醇,目的是及时发现煤气泄漏12. 下列实验操作符合规范的是( )A、塞紧橡胶塞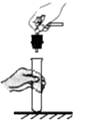 B、铁丝在O2 中燃烧
B、铁丝在O2 中燃烧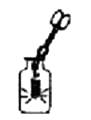 C、闻气体的气味
C、闻气体的气味 D、称量NaCl质量
D、称量NaCl质量 13. 下列关于金属的说法正确的是( )
13. 下列关于金属的说法正确的是( )
A、铝元素在地壳中含量最多,使用也最早 B、不锈钢的抗腐蚀性强于纯铁,硬度小于纯铁 C、灯泡里的灯丝常用钨制成 D、地球上金属矿物资源储量有限,可再生14. 根据下列实验方案进行实验,能达到相应实验目的的是( )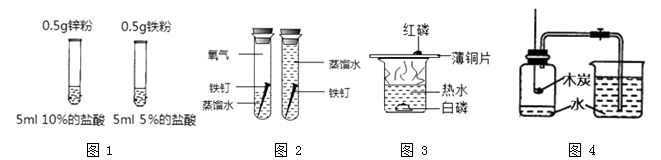 A、图 1 比较 Zn 和 Fe 的金属活动性强弱 B、图 2 探究铁钉生锈时 O2 是否参与反应 C、图 3 比较红磷和白磷的着火点 D、图 4 测定空气中 O2 的含量
A、图 1 比较 Zn 和 Fe 的金属活动性强弱 B、图 2 探究铁钉生锈时 O2 是否参与反应 C、图 3 比较红磷和白磷的着火点 D、图 4 测定空气中 O2 的含量二、填空题
-
15. 在宏观、微观和符号之间建立联系,是化学学科的特点,如图是某化学反应的微观过程示意图(“
 ”表示氧原子,“〇”表示氢原子).
”表示氧原子,“〇”表示氢原子).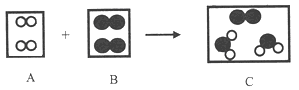 (1)、从宏观角度看,物质C属于(选填“混合物”或“纯净物”);(2)、以上变化的基本反应类型是;(3)、从微观角度看,物质B是由构成的(选填“分子”或“原子”或“离子”);(4)、参加反应的A与B的微粒个数比为 .16. 钒被誉为“合金中的维生素”。钒元素的部分信息如图所示。请回答下列问题:
(1)、从宏观角度看,物质C属于(选填“混合物”或“纯净物”);(2)、以上变化的基本反应类型是;(3)、从微观角度看,物质B是由构成的(选填“分子”或“原子”或“离子”);(4)、参加反应的A与B的微粒个数比为 .16. 钒被誉为“合金中的维生素”。钒元素的部分信息如图所示。请回答下列问题:
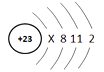 (1)、钒原子的质子数为 , x=。
(1)、钒原子的质子数为 , x=。
(2)、钒属于(填“金属”或“非金属”)元素;钒的相对原子质量为。
17. 请根据下图回答问题:



① 关闭阀门 ② 浇水 ③加水 ④火焰飞溅
(1)、图①和②两种灭火方式的原理分别是:① , ②。
(2)、图③是往燃烧的油锅里加水,结果不但没有熄灭锅里的水,还造成图④的后果,其原因是: , , 使燃烧更猛烈;正确熄灭油锅里火焰的方法是。
18. 实验室根据工业炼铁的原理设计了如图所示装置进行实验。请回答: (1)、主要成分为氧化铁的矿石名称为;
(1)、主要成分为氧化铁的矿石名称为;图中还原氧化铁的化学方程式为:
(2)、“加热”和“通气”(通入CO)的操作顺序是。19. 化学与我们的生活息息相关。
(1)、目前,人类以化石燃料为主要能源。煤、和天然气是常见的化石燃料。天然气充分燃烧的化学方程式为。
(2)、洁净的空气对人类非常重要。下列做法不利于保护大气的是__________(填字母序号)。A、燃煤取暖改为天然气供暖 B、积极植树造林 C、工业废气处理后排放 D、焚烧落叶和垃圾(3)、为减少温室气体二氧化碳的排放,可以将二氧化碳进行转化。下图为该反应的微观示意图,根据图示回答下列问题。反应前
反应后

A
B
C
D

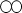

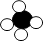
以上4种质中不属于氧化物的是(填字母序号)。
三、推断题
-
20. A﹣J都是初中化学中的常见物质,其中D、E对维持自然界生命活动至关重要,A、B为黑色固体,C是红色金属单质.它们的相互转化关系如图所示.
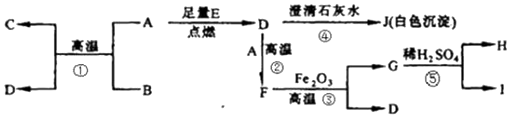
请回答下列问题:
(1)、写出下列物质的化学式:B;D;J;G;(2)、写出反应①②④的化学方程式①;②;④ .四、实验探究题
-
21. 根据下图回答有关问题。
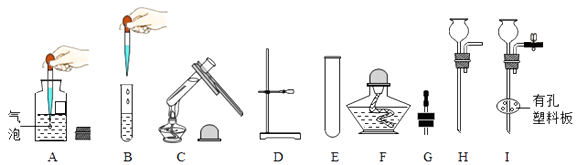 (1)、仪器E的名称为。
(1)、仪器E的名称为。
(2)、图A~C是常见实验基本操作。其中正确的是(填序号);请选择一个有错误的操作写出改正方法:。
(3)、选择仪器D~I完成下列实验操作:①用KMnO4制备O2 , 应选仪器(填序号),其化学反应方程式为;
②用大理石与稀盐酸反应制备CO2并使反应随时发生或停止,应选仪器 ,
其反应方程式为。
(4)、下图是以锌粒和稀硫酸反应制备H2 , 并用排水法收集。请把图补画完整。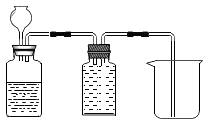
五、科学探究题
-
22. 碲(Te)被誉为“现代工业、国防与尖端技术的维生素,创造人间奇迹的桥梁”。实验室模拟提取碲的一个实验是:取某含碲溶液于烧瓶中,加入适量的NaCl,加热到一定温度,持续通入SO2 , 待反应一段时间,过滤得到粗碲。
(1)、反应的总反应方程式为TeOSO4 + 2SO2 + 3X Te↓+ 3H2SO4 , 则X为(填化学式)(2)、为探究获得较高粗碲沉淀率的反应条件,某研究小组在控制NaCl浓度和SO2流量不变的条件下,进行下述对比试验,数据如下:实验
温度/℃
反应时间/h
粗碲沉淀率/%
a
65
3.0
65.0
b
80
3.0
98.9
c
80
2.0
98.9
d
90
2.0
97.0
①该小组研究的反应条件是和。
②实验a和b的目的是。
③在上述四组实验中,最佳的反应条件是℃和h。
④为了提升设备利用效率和节约能源,可进一步优化反应条件测定粗碲沉淀率。若再设计对比实验,选择的反应条件还可以是(填选项)。
A.80℃,1.5h B.80℃,2.5h C.70℃,2.0h D.95℃,2.0h
六、计算题
-
23. 阿斯匹林(分子式为C9H8O4)是一种常用解热镇痛药,用于治疗感冒、发烧、头痛等疾病。某阿斯匹林肠溶片说明书的部分内容如图所示。
 (1)、阿斯匹林的相对分子质量是 , 其中氢、氧元素的质量比是;(2)、阿斯匹林中碳元素的质量分数;25mg阿斯匹林中含碳元素的质量;(3)、治疗不稳定性心绞痛时,病人每天服用阿斯匹林肠溶片的最大量是片。
(1)、阿斯匹林的相对分子质量是 , 其中氢、氧元素的质量比是;(2)、阿斯匹林中碳元素的质量分数;25mg阿斯匹林中含碳元素的质量;(3)、治疗不稳定性心绞痛时,病人每天服用阿斯匹林肠溶片的最大量是片。七、综合题
-
24. 化学兴趣小组的同学欲除去某FeCl2溶液中混有的CuCl2杂质,实验操作步骤如下:
(1)、①在混合溶液中加入过量的 粉(只有一个正确选项,选填字母),搅拌,使其充分反应:
A、铁 B、铜 C、银②过滤,得到FeCl2溶液和金属混合物.(2)、该小组同学欲继续探究上述②得到的金属混合物中Cu的质量分数,将该金属混合物洗涤、干燥,称得其质量为28.0g.向此金属混合物中逐滴滴加稀盐酸,产生氢气的质量与加入稀盐酸溶液的质量关系如图所示,完成下列问题: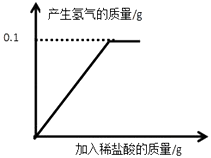
①计算该金属混合物中Cu的质量分数.(请根据化学方程式写出完整的计算步骤)
②该实验中,有同学认为还可以通过测定其他数据来计算Cu的质量分数,实验时他需要测定的实验数据应是 .
-
-
-
-