北京市丰台2017-2018学年九年级上学期化学期末考试试卷
试卷日期:2018-02-07 考试类型:期末考试
一、单选题
-
1. 1.能闻到花香的原因是( )A、分子的质量很小 B、分子间有间隔 C、分子在不断运动 D、分子由原子构成2. 下列物质在氧气中燃烧,火星四射并生成黑色固体的是( )A、硫磺 B、镁条 C、红磷 D、铁丝3. 地壳中含量最多的元素是( )A、Fe B、O C、Si D、Al4. 下列物质中属于氧化物的是( )A、Al2O3 B、O2 C、NaCl D、Mg(OH)25. 下列物质中,表示2个氢分子的是( )A、H2 B、2H2 C、2H D、2H+6. 紫薯(如图)富含淀粉、蛋白质、维生素、钾、铁、钙、硒等,具有特殊的保健功能。其中的钾、铁、钙、硒指的是( )

 A、单质 B、原子 C、分子 D、元素7. 下列图示的实验操作中,不正确的是 ( )A、
A、单质 B、原子 C、分子 D、元素7. 下列图示的实验操作中,不正确的是 ( )A、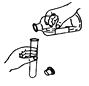 倾倒液体
B、
倾倒液体
B、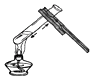 加热液体
C、
加热液体
C、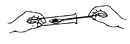 取用固体药品
D、
取用固体药品
D、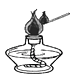 点燃酒精灯
8. 下列金属的活动性最强的是( )A、Al B、Mg C、Zn D、Fe9. 化学变化前后发生改变的是( )A、元素种类 B、原子个数 C、分子种类 D、原子质量10. 已知一种氧原子,原子核内有8个质子和10个中子,则该氧原子中核外电子数为( )A、2 B、8 C、10 D、1811. 下图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列有关该实验的说法中,正确的是 ( )
点燃酒精灯
8. 下列金属的活动性最强的是( )A、Al B、Mg C、Zn D、Fe9. 化学变化前后发生改变的是( )A、元素种类 B、原子个数 C、分子种类 D、原子质量10. 已知一种氧原子,原子核内有8个质子和10个中子,则该氧原子中核外电子数为( )A、2 B、8 C、10 D、1811. 下图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列有关该实验的说法中,正确的是 ( ) A、红磷熄灭后应立刻打开弹簧夹 B、实验前要检查装置的气密性 C、最终瓶中剩余的气体是纯净的氮气 D、实验时,只取用极少量红磷,可减少污染且不影响实验结果12. 下列物质的用途中,利用了其化学性质的是( )A、氧气用于医疗急救 B、干冰用于人工降雨 C、铜用作制导线 D、黄金用作制首饰13. 用微观示意图表示空气的主要成分(已知在同温同压下,气体的体积之比等于分子个数之比),下图中最合理的是( )
A、红磷熄灭后应立刻打开弹簧夹 B、实验前要检查装置的气密性 C、最终瓶中剩余的气体是纯净的氮气 D、实验时,只取用极少量红磷,可减少污染且不影响实验结果12. 下列物质的用途中,利用了其化学性质的是( )A、氧气用于医疗急救 B、干冰用于人工降雨 C、铜用作制导线 D、黄金用作制首饰13. 用微观示意图表示空气的主要成分(已知在同温同压下,气体的体积之比等于分子个数之比),下图中最合理的是( ) A、
A、 B、
B、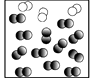 C、
C、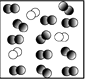 D、
D、 14. 下列实验操作一定能达到实验目的的是( )
14. 下列实验操作一定能达到实验目的的是( )选项
实验目的
实验操作
A
比较空气和呼出气体中CO2含量
分别伸入燃着的木条
B
鉴别铁粉和碳粉
观察颜色
C
除去CO2气体中的CO气体
点燃气体
D
鉴别CO和H2
分别点燃,在火焰上方罩一干冷烧杯
A、A B、B C、C D、D15. 工业上常用高温煅烧石灰石的方法来制得生石灰,发生的反应为CaCO3 CaO + CO2↑。现取一定量的石灰石样品进行煅烧(假设杂质质量不变),某变量y随时间的变化趋势如下图所示。则纵坐标表示的是( )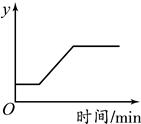 A、生成CO2的体积 B、生成CaO的质量 C、固体中杂质的质量分数 D、固体中氧元素的质量
A、生成CO2的体积 B、生成CaO的质量 C、固体中杂质的质量分数 D、固体中氧元素的质量二、简答题
-
16. 中午,同学们在学校用餐。
(1)、下列食物中,能提供蛋白质的是(填字母序号)。为了防止佝偻病,需要补充富含元素的食品 (2)、二氧化碳可用于制作碳酸饮料,写出其中发生反应的化学方程式。(3)、餐厅中有自热米饭,其发热的原理是利用了生石灰与水反应放热,写出发生反应的化学方程式。(4)、食堂要做“翡翠”饺子,可将菠菜榨汁,通过操作将菜渣与菜汁分离,用菜汁和面。17. 阅读下面科普短文。
(2)、二氧化碳可用于制作碳酸饮料,写出其中发生反应的化学方程式。(3)、餐厅中有自热米饭,其发热的原理是利用了生石灰与水反应放热,写出发生反应的化学方程式。(4)、食堂要做“翡翠”饺子,可将菠菜榨汁,通过操作将菜渣与菜汁分离,用菜汁和面。17. 阅读下面科普短文。2017年,我国在南海北部神狐海域进行的可燃冰试采获得成功。你对可燃冰有多少了解呢?
什么是可燃冰?可燃冰外观像冰,主要含甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等气体。甲烷水合物的分子结构就像一个一个由若干水分子组成的笼子,每个笼子里“关”一个甲烷分子。可燃冰是怎样形成的?可燃冰的形成要满足三个条件:⑴温度不能太高。⑵压力要足够大。⑶要有甲烷气源。在上述三个条件都具备的情况下,天然气可与水生成甲烷水合物,分散在海底岩层的空隙中。甲烷水合物能稳定存在的压强和温度范围如下图所示:
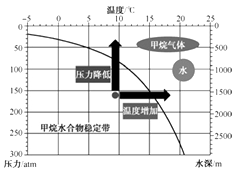
为什么开采困难?可燃冰开采的最大难点是保证甲烷气体不泄露、不引发温室效应,甲烷引发的温室效应比二氧化碳厉害10至20倍,可燃冰一离开海床便迅速分解,容易发生喷井意外,还可能会破坏地壳稳定平衡,引发海底塌方,导致大规模海啸。
可燃冰有哪些用途?一体积可燃冰可储载约164倍体积的甲烷气体,具有能量高、燃烧值大等优点,而且储量丰富,因而被各国视为未来石油天然气的替代能源。甲烷还是重要的化工原料,可制造炭黑、乙炔、氰化氢等。依据文章内容,回答下列问题:
(1)、可燃冰属于(填“纯净物”或“混合物”)。(2)、可燃冰形成的适宜条件是____________。A、高温高压 B、低温高压 C、低温低压(3)、可燃冰作为能源的优点是。(4)、甲烷燃烧的化学方程式为。(5)、有关可燃冰的说法正确的是_________。A、可燃冰不是冰 B、可燃冰开采时若出现差错,可能引发严重的环境灾害 C、在1atm和25℃时,可燃冰能稳定存在18. 氢能是理想的清洁能源。以太阳能为热源,经由铁氧化合物循环分解水的过程如下: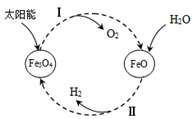 (1)、反应Ⅰ的基本反应类型为。(2)、写出在一定条件下发生的反应Ⅱ的化学方程式。(3)、在上述循环过程中,最终得到的产品是。19. 下图实验装置被称为“人工树叶”。产物C3H8O是重要的化工原料,也可用作燃料。
(1)、反应Ⅰ的基本反应类型为。(2)、写出在一定条件下发生的反应Ⅱ的化学方程式。(3)、在上述循环过程中,最终得到的产品是。19. 下图实验装置被称为“人工树叶”。产物C3H8O是重要的化工原料,也可用作燃料。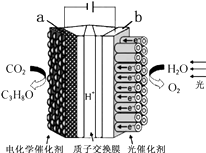 (1)、C3H8O中,碳氢原子的个数比为。(2)、该装置被称为“人工树叶”的主要原因是____。A、它外形像树叶 B、它模拟了植物的光合作用20. 根据下图装置回答实验室制取氧气及氧气性质的相关问题。
(1)、C3H8O中,碳氢原子的个数比为。(2)、该装置被称为“人工树叶”的主要原因是____。A、它外形像树叶 B、它模拟了植物的光合作用20. 根据下图装置回答实验室制取氧气及氧气性质的相关问题。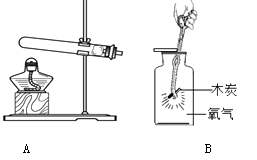 (1)、用高锰酸钾制氧气,反应的化学方程式为。(2)、用向上排空气法收集氧气,验满的操作是。(3)、B中观察到木炭剧烈燃烧,发出白光,说明氧气具有的性质是。21. 利用下图装置研究二氧化碳的性质。
(1)、用高锰酸钾制氧气,反应的化学方程式为。(2)、用向上排空气法收集氧气,验满的操作是。(3)、B中观察到木炭剧烈燃烧,发出白光,说明氧气具有的性质是。21. 利用下图装置研究二氧化碳的性质。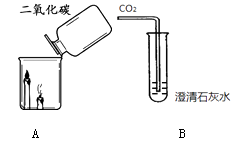 (1)、实验A的现象体现了二氧化碳的性质是。(2)、实验B中,二氧化碳与澄清石灰水反应的化学方程式为。
(1)、实验A的现象体现了二氧化碳的性质是。(2)、实验B中,二氧化碳与澄清石灰水反应的化学方程式为。三、填空题
-
22. 午餐后,老师对学生们进行了安全教育。(1)、根据图标填空:A , B , C。
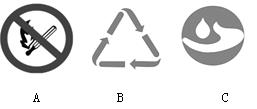 (2)、下列说法正确的是_____。A、电器着火,立即用水扑灭。 B、禁止携带易燃易爆品乘坐地铁。 C、通过降低可燃物的着火点可以灭火。
(2)、下列说法正确的是_____。A、电器着火,立即用水扑灭。 B、禁止携带易燃易爆品乘坐地铁。 C、通过降低可燃物的着火点可以灭火。四、综合题
-
23. 到达目的地后,同学们开始了参观,钢铁煤炭行业“去产能”效果明显。
 (1)、除煤之外,和天然气也是化石燃料。(2)、工业上用一氧化碳和赤铁矿(主要成分Fe2O3)炼铁的化学方程式为。(3)、煤炭“去产能”是指为了解决煤炭生产过剩,从而对企业生产能力进行整改。下列做法有利于煤矿行业去产能的是_________。A、关闭一些技术落后的小煤矿业,减少煤炭产量 B、将一些煤矿企业转型为新能源企业 C、全面禁止生产煤炭24. “绿水青山”就是“金山银山”。(1)、在汽车尾气的排放管安装催化转化器,可在一定程度上实现节能减排。
(1)、除煤之外,和天然气也是化石燃料。(2)、工业上用一氧化碳和赤铁矿(主要成分Fe2O3)炼铁的化学方程式为。(3)、煤炭“去产能”是指为了解决煤炭生产过剩,从而对企业生产能力进行整改。下列做法有利于煤矿行业去产能的是_________。A、关闭一些技术落后的小煤矿业,减少煤炭产量 B、将一些煤矿企业转型为新能源企业 C、全面禁止生产煤炭24. “绿水青山”就是“金山银山”。(1)、在汽车尾气的排放管安装催化转化器,可在一定程度上实现节能减排。A、B、C、D表示4种物质,其微观示意图见下表。
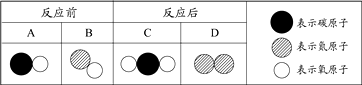
下列说法正确的是_______(填字母序号)。
A、四种物质均由分子构成 B、该反应属于置换反应 C、该反应中,C、D两种物质的微粒个数比为1:1(2)、引起酸雨的主要物质是SO2和NO2 , SO2中硫元素的化合价为。(3)、下列做法中,不符合“尊重自然、自觉践行绿色生活”倡议的是_____。A、乘坐公共交通工具出行 B、使用一次性餐具 C、自带水杯出行 D、对垃圾进行分类五、实验探究题
-
25. 水是生命之源,电解水实验如下图所示。
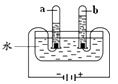 (1)、试管b中的气体为。(2)、该反应的化学方程式为。26. 利用压气蒸馏的方法可以将海水淡化,工作原理如下图所示:
(1)、试管b中的气体为。(2)、该反应的化学方程式为。26. 利用压气蒸馏的方法可以将海水淡化,工作原理如下图所示: (1)、蒸发器中发生的是变化(填“物理”或“化学”) 。(2)、浓盐水中含有NaCl、MgCl2、CaCl2等,MgCl2中镁、氯元素的质量比为。27. 利用下图装置进行实验。
(1)、蒸发器中发生的是变化(填“物理”或“化学”) 。(2)、浓盐水中含有NaCl、MgCl2、CaCl2等,MgCl2中镁、氯元素的质量比为。27. 利用下图装置进行实验。实验装置
实验1 探究燃烧的条件
实验2 制取二氧化碳

Ⅰ.燃烧匙中放置一小块白磷(着火点为40℃),装置中盛放80℃的热水(浸没白磷)。
Ⅱ.打开K,从导管口鼓入空气至白磷露出水面,关闭K。
Ⅰ.燃烧匙中盛有大理石,装置中盛放一定量的稀盐酸(浸没大理石)。
Ⅱ.打开K,收集二氧化碳。
Ⅲ.……
(1)、实验1中,白磷燃烧的化学方程式为;(2)、实验1中,能证明燃烧需要与氧气接触的实验现象是;(3)、实验2中,制取二氧化碳的化学方程式为;(4)、实验2中,为使反应停止,Ⅲ中的操作是。六、科学探究题
-
28. 利用下图装置探究金属的活动性顺序。
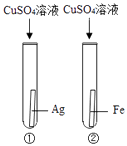 (1)、实验中发生反应的化学方程式为。(2)、实验中观察到现象,验证了三种金属的活动性。29. 过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。(1)、I.不稳定性
(1)、实验中发生反应的化学方程式为。(2)、实验中观察到现象,验证了三种金属的活动性。29. 过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。(1)、I.不稳定性如下图所示进行实验,过氧化氢分解的化学方程式为 , 产生3.2g O2时分解的过氧化氢的质量为 g。
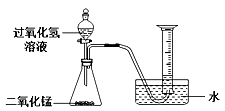 (2)、能用排水法收集O2的原因是。(3)、探究温度对过氧化氢分解速率的影响
(2)、能用排水法收集O2的原因是。(3)、探究温度对过氧化氢分解速率的影响同学们进行了如下的实验,实验数据如下表:
实验序号
①
②
③
H2O2溶液的浓度%
30
30
30
H2O2溶液的体积/mL
6
6
6
温度/℃
20
35
55
MnO2的用量/g
0
0
0
收集O2的体积/mL
0
1.9
7.8
反应时间
40min
40min
40 min
由此得出的结论是。
(4)、Ⅱ.腐蚀性【查阅资料】H2O2溶液有腐蚀性。
【进行实验】
将铜片分别浸泡在3种溶液中进行实验,如下表。
编号
①
②
③
实验
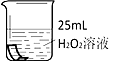
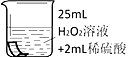
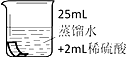
一段时间后的现象
无明显变化
溶液变蓝,缓慢产生细小气泡
无明显变化
【解释与结论】
实验①的作用是。
(5)、铜片被腐蚀的反应如下,补全该反应的化学方程式。Cu + H2O2+ H2SO4= CuSO4 +。
(6)、【反思交流】某同学提出,实验②中,除发生(5)的反应外,还发生了一个反应导致有细小气泡产生,该反应的反应物为。
-