广东省深圳市罗湖区2017-2018学年九年级上学期化学期末考试试卷
试卷日期:2018-02-07 考试类型:期末考试
一、选择题
-
1. 下列化学用语及其含义正确的是( )A、O3:三个氧原子 B、CO:一氧化碳 C、FeCl2:氯化亚铁 D、 :氢气中氢元素的化合价为+12. 下图所示实验操作不正确的是( )A、过滤
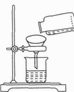 B、取固体粉末
B、取固体粉末 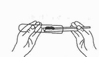 C、熄灭酒精灯
C、熄灭酒精灯 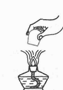 D、滴加液体
D、滴加液体 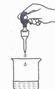 3. 用下图装置测定空气中氧气的含量,物质R应该选用( )
3. 用下图装置测定空气中氧气的含量,物质R应该选用( ) A、铁片 B、红磷 C、木炭 D、硫粉4. 水是重要资源,下列说法正确的是( )A、活性炭的吸附作用可使海水转化为淡水 B、水中的Ca2+、Mg2+可用过滤的方法除去 C、电解水得到的H2和O2 , 质量比为2:1 D、液态水变成水蒸气,分子间间隔增大5. 根据如图有关信息判断,下列说法正确的是( )
A、铁片 B、红磷 C、木炭 D、硫粉4. 水是重要资源,下列说法正确的是( )A、活性炭的吸附作用可使海水转化为淡水 B、水中的Ca2+、Mg2+可用过滤的方法除去 C、电解水得到的H2和O2 , 质量比为2:1 D、液态水变成水蒸气,分子间间隔增大5. 根据如图有关信息判断,下列说法正确的是( )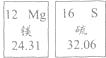 A、在元素周期表中,镁元素和硫元素属于同一族 B、镁离子的结构示意图为
A、在元素周期表中,镁元素和硫元素属于同一族 B、镁离子的结构示意图为 C、硫原子的质子数和电子数之和是16
D、硫化镁(MgS)中镁的质量分数约为43%
6. 如图是某化学反应的微观示意图(黑白小圈分别表示不同的原子),从图中获得的信息错误的是( )
C、硫原子的质子数和电子数之和是16
D、硫化镁(MgS)中镁的质量分数约为43%
6. 如图是某化学反应的微观示意图(黑白小圈分别表示不同的原子),从图中获得的信息错误的是( )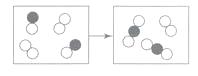 A、该图表示的是一个化合反应 B、该图表示反应物和生成物都有两种 C、原子是化学变化中的最小粒子 D、该反应中,反应物、生成物的粒子个数比可表示为2:1:27. 下列有关物质燃烧时实验现象的描述中,正确的是( )A、红磷在空气中燃烧产生大量的烟雾 B、硫在空气中燃烧发出蓝紫色火焰,产生有刺激性气味的气体 C、木炭在氧气中比在空气中燃烧更剧烈,发出白光 D、铁丝在氧气中燃烧生成黑色的四氧化三铁固体8. 分类法是学习和研究化学的常用方法,下列分类正确的是( )A、化石燃料:煤、石油、天然气 B、空气污染物:CO2、NO2、SO2 C、净化水的方法:沉降、过滤、吸附、电解 D、基本反应类型:化合反应、置换反应、氧化反应9. 某气体可能含有水蒸气、CO、CO2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过装置( )
A、该图表示的是一个化合反应 B、该图表示反应物和生成物都有两种 C、原子是化学变化中的最小粒子 D、该反应中,反应物、生成物的粒子个数比可表示为2:1:27. 下列有关物质燃烧时实验现象的描述中,正确的是( )A、红磷在空气中燃烧产生大量的烟雾 B、硫在空气中燃烧发出蓝紫色火焰,产生有刺激性气味的气体 C、木炭在氧气中比在空气中燃烧更剧烈,发出白光 D、铁丝在氧气中燃烧生成黑色的四氧化三铁固体8. 分类法是学习和研究化学的常用方法,下列分类正确的是( )A、化石燃料:煤、石油、天然气 B、空气污染物:CO2、NO2、SO2 C、净化水的方法:沉降、过滤、吸附、电解 D、基本反应类型:化合反应、置换反应、氧化反应9. 某气体可能含有水蒸气、CO、CO2中的一种或几种.为了确定其成分,最佳的实验方案是将气体依次通过装置( ) A、甲、乙、丙 B、丙、乙、甲 C、丙、甲、乙 D、乙、甲、丙10. 下列方法或试剂能达到除杂目的的是( )
A、甲、乙、丙 B、丙、乙、甲 C、丙、甲、乙 D、乙、甲、丙10. 下列方法或试剂能达到除杂目的的是( )物质(括号内是杂质)
方法或试剂
A
FeSO4(CuSO4)
Fe
B
Fe(Cu)
CuCl2
C
CO2(CO)
点燃
D
CaO(CaCO3)
水
A、A B、B C、C D、D二、非选择题
-
11. 工业上用钛铁矿(主要成分FeTiO3)制备金属钛的一种工艺流程如下图所示(部分产物略):
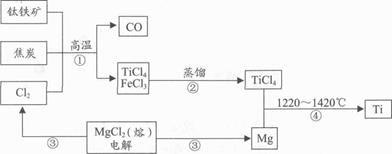 (1)、钛铁矿的主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为。(2)、反应①产生的CO是水煤气的主要成分,它燃烧时的火焰呈色,检验CO2的化学方法是(书写化学方程式)。(3)、在实验室中进行步骤②操作,所需的玻璃仪器有、蒸馏烧瓶、冷凝管、温度汁、尾接管、锥形瓶等。(4)、反应④属于置换反应,它的化学方程式为 , 该反应在氩气中进行的原因是防止高温下(填化学式,一种即可)与氧气发生反应。(5)、绿色化学提倡物质循环利用。仔细观察上述流程图,回答:在以上流程中,可循环使用的物质是(填化学式,一种即可)。12. 实验室常采用亚硫酸钠固体(Na2SO3)与浓硫酸在常温下反应制取SO2 , SO3是一种有毒气体,密度比空气大,易溶于水。
(1)、钛铁矿的主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为。(2)、反应①产生的CO是水煤气的主要成分,它燃烧时的火焰呈色,检验CO2的化学方法是(书写化学方程式)。(3)、在实验室中进行步骤②操作,所需的玻璃仪器有、蒸馏烧瓶、冷凝管、温度汁、尾接管、锥形瓶等。(4)、反应④属于置换反应,它的化学方程式为 , 该反应在氩气中进行的原因是防止高温下(填化学式,一种即可)与氧气发生反应。(5)、绿色化学提倡物质循环利用。仔细观察上述流程图,回答:在以上流程中,可循环使用的物质是(填化学式,一种即可)。12. 实验室常采用亚硫酸钠固体(Na2SO3)与浓硫酸在常温下反应制取SO2 , SO3是一种有毒气体,密度比空气大,易溶于水。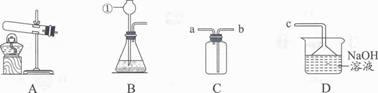 (1)、仪器①的名称是。
(1)、仪器①的名称是。
(2)、实验室制取SO2选择的发生装置是图 (填字母序号)。实验室用该装置还可以制取O2或者CO2 , 分别写出制取这两种气体的化学方程式: , ,前者属于基本反应类型中的。
(3)、用图C所示装置收集SO2时,(填“a”或“b”)端管口进气。图D烧杯中NaOH溶液可以吸收多余SO2 , 生成亚硫酸钠(Na2SO3)和水,则该反应的化学方程式:(填序号)。A.NaOH+SO2=Na2SO3+H2O
B.2NaOH+SO2=Na2SO3+H2O .
C.2NaOH+SO2=Na2SO3
13.(1)、现有三组物质:①Zn、Cu、稀硫酸;②Zn、Cu、MgSO4溶液;③Zn、Cu、AgNO3溶液,用组内物质就能够比较锌和铜的金属活动性的是(填序号);
(2)、相同质量的Fe和Zn分别与一定量的稀H2SO4反应,最终生成的H2质量相等,其中Zn与稀H2SO4的反应情况如下图曲线A所示。
①请用曲线B在上图中表示出Fe与稀H2SO4反应产生气体的情况。
②判断:金属(填“Zn”或“Fe”)一定有剩余。
(3)、若上述反应中消耗了28g的Fe,计算由Fe产生H2的质量。(要求利用化学方程式进行计算,写出过程。)