北京市门头沟区2015-2016学年九年级上册化学期末考试试卷
试卷日期:2018-01-15 考试类型:期末考试
一、单选题
-
1. 物质世界充满了变化,下列变化属于物理变化的是( )A、
 镁条燃烧
B、
镁条燃烧
B、 钢铁生锈
C、
钢铁生锈
C、 酿谷成酒
D、
酿谷成酒
D、 干冰升华
2. 空气中体积分数约占78%的气体是( )A、氮气 B、氧气 C、二氧化碳 D、稀有气体3. “铁强化酱油”中的“铁”是指( )
干冰升华
2. 空气中体积分数约占78%的气体是( )A、氮气 B、氧气 C、二氧化碳 D、稀有气体3. “铁强化酱油”中的“铁”是指( ) A、原子 B、分子 C、单质 D、元素4. 以下饮品不属于溶液的是( )A、
A、原子 B、分子 C、单质 D、元素4. 以下饮品不属于溶液的是( )A、 啤酒
B、
啤酒
B、 酸奶
C、
酸奶
C、 矿泉水
D、
矿泉水
D、 可口可乐
5. 下列属于纯净物的是( )A、加碘食盐 B、蒸馏水 C、氯化钠注射液 D、食醋6. 下列二氧化碳(干冰)的用途中,不正确的是( )A、供给呼吸 B、用作气体肥料 C、生产碳酸饮料 D、用于制造舞台烟雾7. 垃圾分类从我做起。金属饮料罐属于( )
可口可乐
5. 下列属于纯净物的是( )A、加碘食盐 B、蒸馏水 C、氯化钠注射液 D、食醋6. 下列二氧化碳(干冰)的用途中,不正确的是( )A、供给呼吸 B、用作气体肥料 C、生产碳酸饮料 D、用于制造舞台烟雾7. 垃圾分类从我做起。金属饮料罐属于( )
A、 可回收物
B、
可回收物
B、 有害垃圾
C、
有害垃圾
C、 厨余垃圾
D、
厨余垃圾
D、 其他垃圾
8. 下列物质的用途中,主要利用其物理性质的是( )A、液氮用作制冷剂 B、天然气用作燃料 C、氧气用于气焊 D、氢气用作清洁能源9. 铝是重要的金属元素。右图为地壳中各元素含量分布图,表示铝元素的是( )
其他垃圾
8. 下列物质的用途中,主要利用其物理性质的是( )A、液氮用作制冷剂 B、天然气用作燃料 C、氧气用于气焊 D、氢气用作清洁能源9. 铝是重要的金属元素。右图为地壳中各元素含量分布图,表示铝元素的是( )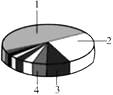 A、1 B、2 C、3 D、410. 下列符号中,表示两个氧分子的是( )A、O2 B、2O C、2O2 D、O2-11. 含氟牙膏对牙齿有保护作用.一种氟原子核内有9个质子和10个中子,该原子的核外电子数为( )A、7 B、9 C、10 D、1912. 海水淡化可采用膜分离技术。如右图所示,对淡化膜右侧的海水加压,水分子可透过淡化膜进入左侧淡水池,而海水中各种离子不能通过淡化膜,从而得到淡化水。对加压后右侧海水成分的变化分析正确的( )
A、1 B、2 C、3 D、410. 下列符号中,表示两个氧分子的是( )A、O2 B、2O C、2O2 D、O2-11. 含氟牙膏对牙齿有保护作用.一种氟原子核内有9个质子和10个中子,该原子的核外电子数为( )A、7 B、9 C、10 D、1912. 海水淡化可采用膜分离技术。如右图所示,对淡化膜右侧的海水加压,水分子可透过淡化膜进入左侧淡水池,而海水中各种离子不能通过淡化膜,从而得到淡化水。对加压后右侧海水成分的变化分析正确的( )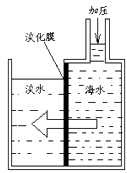 A、溶质质量增加 B、溶剂质量减少 C、溶液质量不变 D、溶质质量分数减少13. 下列做法中,不恰当的是( )A、电器短路起火,立即切断电源 B、炒菜时油锅着火,立即用水浇灭 C、酒精灯不慎打翻起火,立即用湿抹布盖灭 D、室内发生天然气泄漏时,立即关闭阀门并开窗通风14. 二氧化碳能用来灭火的原因是( )A、二氧化碳能与燃烧的物质发生化学反应 B、二氧化碳溶于水时生成碳酸 C、在一定条件下,二氧化碳可变成“干冰” D、能使可燃物与氧气隔绝15. 下图是氯原子的结构示意图。下列说法不正确的是( )
A、溶质质量增加 B、溶剂质量减少 C、溶液质量不变 D、溶质质量分数减少13. 下列做法中,不恰当的是( )A、电器短路起火,立即切断电源 B、炒菜时油锅着火,立即用水浇灭 C、酒精灯不慎打翻起火,立即用湿抹布盖灭 D、室内发生天然气泄漏时,立即关闭阀门并开窗通风14. 二氧化碳能用来灭火的原因是( )A、二氧化碳能与燃烧的物质发生化学反应 B、二氧化碳溶于水时生成碳酸 C、在一定条件下,二氧化碳可变成“干冰” D、能使可燃物与氧气隔绝15. 下图是氯原子的结构示意图。下列说法不正确的是( )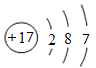 A、氯原子的原子核内质子数为17 B、氯原子的原子核内中子数为17 C、氯原子的核外有三个电子层 D、氯原子的最外层电子数目影响氯元素的化学性质16. 对下列事实解释不正确的是( )
A、氯原子的原子核内质子数为17 B、氯原子的原子核内中子数为17 C、氯原子的核外有三个电子层 D、氯原子的最外层电子数目影响氯元素的化学性质16. 对下列事实解释不正确的是( ) A、A B、B C、C D、D17. X、Y、Z三种物质的溶解度曲线如右图所示。下列叙述中,正确的是( )
A、A B、B C、C D、D17. X、Y、Z三种物质的溶解度曲线如右图所示。下列叙述中,正确的是( )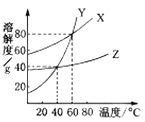 A、40℃时Z的溶解度最大 B、三种物质的饱和溶液,温度由60℃降至40℃时,Y析出的晶体最多 C、40℃时,Z和Y的饱和溶液的溶质质量分数相同 D、40℃时,X、Y、Z的饱和溶液升温至60℃,溶质质量分数X=Y>Z18. 纳米材料具有特殊的性质和功能,纳米二氧化钛(TiO2)参与的光催化反应可使吸附在其表面的甲醛等物质被氧化,降低空气中有害物质的浓度。正钛酸 在一定条件下分解失水可制得纳米TiO2。下列说法不正确的是( )
A、40℃时Z的溶解度最大 B、三种物质的饱和溶液,温度由60℃降至40℃时,Y析出的晶体最多 C、40℃时,Z和Y的饱和溶液的溶质质量分数相同 D、40℃时,X、Y、Z的饱和溶液升温至60℃,溶质质量分数X=Y>Z18. 纳米材料具有特殊的性质和功能,纳米二氧化钛(TiO2)参与的光催化反应可使吸附在其表面的甲醛等物质被氧化,降低空气中有害物质的浓度。正钛酸 在一定条件下分解失水可制得纳米TiO2。下列说法不正确的是( )
A、甲醛对人体健康有害 B、纳米TiO2添加到墙面涂料中,可消除甲醛 C、纳米TiO2与普通的TiO2的性质、功能完全相同 D、制备纳米TiO2的反应:H4TiO4 TiO2+2H2O19. 实验室制取二氧化碳有以下几个步骤:①按要求装好仪器;②向长颈漏斗中注入盐酸;③向反应器中加入块状石灰石;④检查装置气密性;⑤收集生成的气体。以上操作正确排列顺序为( )
A、①②③④⑤ B、②①④③⑤ C、①④③②⑤ D、①②④③⑤20. 下列图像能正确反映对应变化关系的是( )
A、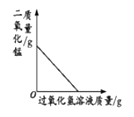 向一定量的二氧化锰中加入过氧化氢溶液
B、
向一定量的二氧化锰中加入过氧化氢溶液
B、 向一定量的水中加入少量氯化钠
C、
向一定量的水中加入少量氯化钠
C、 向一定量石灰石中滴加稀盐酸
D、
向一定量石灰石中滴加稀盐酸
D、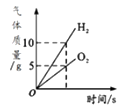 将水通电电解一段时间
将水通电电解一段时间
二、填空题
-
21. 小小是一个爱劳动的初三年级的学生,他决定利用周末休息时间帮妈妈做些事。为父母准备早点,他准备的早点有:鸡蛋、高钙牛奶、面包和苹果。(1)、早点中能提供丰富蛋白质的是。(2)、高钙牛奶可以为人体补充每天所需的钙元素,老年人缺钙会导致的疾病是(填字母序号) 。A、贫血 B、龋齿 C、骨质疏松22. 最近天气雾霾情况严重,小小为准备上班的父母准备了防霾口罩。
 (1)、某品牌口罩的制作材料有:涤纶、活性炭、棉、塑料,其中属于有机合成材料的是。
(1)、某品牌口罩的制作材料有:涤纶、活性炭、棉、塑料,其中属于有机合成材料的是。
(2)、口罩中加入活性炭主要利用活性炭的性。23. 家里开水没有了,小小准备烧一些开水。 (1)、小小发现烧水的水壶中有较多水垢,怀疑家里的水是硬水,他可以通过向自来水中加入加以鉴别。用食醋可以除去水垢,醋的有效成分可用HAc表示,水垢的主要成分是碳酸钙,其反应原理与实验室制取二氧化碳的原理相似,请写出化学反应方程式。(2)、生活中常采用的方法降低水的硬度。24. 整理物品。小小发现家中角落堆积的一些铁丝、铝丝和铜丝。(1)、小小很容易辨别出铜丝,他依据的是;三种金属都可拉成丝状,利用了金属的性。(2)、三种金属都能用来制导线,这是利用了金属的性;小小想验证铝丝具有导热性,可采用的实验方法是。25. 小小整理药品时:
(1)、小小发现烧水的水壶中有较多水垢,怀疑家里的水是硬水,他可以通过向自来水中加入加以鉴别。用食醋可以除去水垢,醋的有效成分可用HAc表示,水垢的主要成分是碳酸钙,其反应原理与实验室制取二氧化碳的原理相似,请写出化学反应方程式。(2)、生活中常采用的方法降低水的硬度。24. 整理物品。小小发现家中角落堆积的一些铁丝、铝丝和铜丝。(1)、小小很容易辨别出铜丝,他依据的是;三种金属都可拉成丝状,利用了金属的性。(2)、三种金属都能用来制导线,这是利用了金属的性;小小想验证铝丝具有导热性,可采用的实验方法是。25. 小小整理药品时:
(1)、小小发现一瓶过氧化氢消毒液,用于清洗伤口时会出现泡沫,原因是(用化学方程式解释)。(2)、小小还发现了一盒头孢地尼分散片,主要成分头孢地尼的化学式为C14H13N5O5S2 , 属于(填“有机物”或“无机物”) , 其中碳、氧元素质量比为。26. 能源是人类生存和发展的基础,能源成为人们日益关注的问题。
(1)、化石燃料包括煤、、天然气等,这些都是重要的能源;目前正在利用和开发的新能源有核能、生物质能、 (填一种)等。(2)、发射卫星的火箭可使用液氢作燃料,液氢在液氧中燃烧的化学方程式为。(3)、物质R是一种可再生绿色能源,其燃烧的化学方程式为R+3O2 2CO2+3H2O,则R的化学式为。27. 2015年8月12日晚,天津东疆保税港区瑞海国际物流有限公司危险品仓库发生爆炸,造成巨大损失。一些物质如“电石”、“氰化钠”等由此得到了人们的广泛关注。电石是碳化钙(CaC2)的简称,遇水立即发生激烈反应,生成乙炔(C2H2)和糊状的强碱氢氧化钙,并放出热量。乙炔在空气中受热、震动、电火花等都可引发爆炸。所以电石干燥时不易燃,一旦遇水或湿气就麻烦了。如果此时还用水来扑灭电石着的火,那就要发生爆炸性灾害。
氰化钠(NaCN)又名山奈,是有剧毒的无机物,有微弱的苦杏仁味。氰化钠极易水解,产生剧毒易燃的氰化氢(HCN)。氰化氢标准状态下为无色透明液体,易挥发,具有苦杏仁气味。能与乙醇、乙醚、甘油、氨、苯、氯仿和水等混溶。灭火剂:干粉、抗溶性泡沫、二氧化碳。用水灭火无效,但须用水保持火场容器冷却。氰化氢主要应用于电镀业(镀铜、镀金、镀银)、采矿业(提取金银),船舱、仓库的烟熏灭鼠,制造各种树脂单体,如丙烯酸树酯、甲基丙烯酸树酯等行业。
(1)、氰化钠水解的产物有两种,除了氰化氢气体,另外的物质中一定含元素。(2)、氰化氢的物理性质有:。(3)、氰化氢的化学性质:。(4)、电石保存时的注意事项28. 下图是工业利用海水提取粗盐的过程。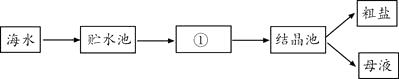 (1)、图中①是(填“蒸发”或“冷却”)池。(2)、在①中,海水中氯化钠的质量分数逐渐(填“变大”或“变小”)。(3)、母液为氯化钠的(填“饱和”或“不饱和”)溶液。29. 质量守恒定律是一条重要规律。请利用该规律的相关知识回答下列问题。
(1)、图中①是(填“蒸发”或“冷却”)池。(2)、在①中,海水中氯化钠的质量分数逐渐(填“变大”或“变小”)。(3)、母液为氯化钠的(填“饱和”或“不饱和”)溶液。29. 质量守恒定律是一条重要规律。请利用该规律的相关知识回答下列问题。
(1)、蜡烛在空气中燃烧时生成二氧化碳和水。由此判断蜡烛中一定含有的元素是(填元素符号),判断的依据是(用微粒的观点解释)。
(2)、某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热(提示:生成氧化铜)并冷却后再次称量,其质量为m2g,则m1m2(填“>”、“<”或“=”),产生这一结果的原因是。(3)、在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表。关于此反应的认识正确的是(填字母序号)。物质
X
Y
Z
W
反应前的质量(g)
2
1
16
16
一段时间后的质量(g)
17
m
6
11
A.m=1 B.该反应为分解反应
C.X与Z的化学计量数之比是3:2 D.若该反应充分进行,反应后W仍有剩余
30. 根据下图回答问题。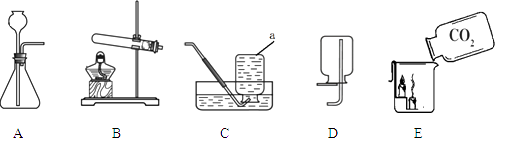 (1)、实验室利用高锰酸钾制备氧气时,选用的发生和收集装置依次是(填字母序号) , 化学反应方程式是。(2)、实验室利用装置制取二氧化碳,化学反应方程式是。E中观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的物理性质。
(1)、实验室利用高锰酸钾制备氧气时,选用的发生和收集装置依次是(填字母序号) , 化学反应方程式是。(2)、实验室利用装置制取二氧化碳,化学反应方程式是。E中观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的物理性质。
31. 水在化学实验中的作用不可忽视,下图中四个实验分别用到水。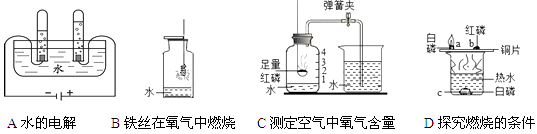 (1)、实验A中水作用是。(2)、实验B中水的作用是。(3)、实验C通过烧杯中的水进入集气瓶中的体积可得出的结论。(4)、实验D中水的作用是提供热量和。32. “去除粗盐中难溶性杂质并计算产率”的实验操作如下图所示:
(1)、实验A中水作用是。(2)、实验B中水的作用是。(3)、实验C通过烧杯中的水进入集气瓶中的体积可得出的结论。(4)、实验D中水的作用是提供热量和。32. “去除粗盐中难溶性杂质并计算产率”的实验操作如下图所示:A.溶解
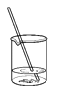 B.蒸发
B.蒸发  C.过滤
C.过滤 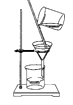 (1)、正确的操作顺序是:称量粗盐质量、(填序号)、称量精盐质量、计算。(2)、操作A中,用玻璃棒不断搅拌的目的是;操作B中用玻璃棒不断搅拌的目的是。(3)、称量精盐质量时,将所得精盐放置于托盘中的纸上,天平指针偏左,合理的操作是 。A、增加砝码或游码 B、增加药品 C、减少砝码或游码 D、减少药品(4)、若实验后发现产率偏低,可能的原因有 。A、滤纸破损 B、蒸发时有固体溅出 C、溶解时加入水不足量,部分盐没有溶解 D、将盐从蒸发皿转移到天平上称量时,没有转移干净33. 用下图所示装置测定空气中氧气的体积分数,实验时先在实际容积为250mL 的集气瓶中装进50mL的水,在粗铜丝末端的铜勺中放足量白磷,按图连好仪器,点燃酒精灯加热铜丝一端,白磷燃烧。
(1)、正确的操作顺序是:称量粗盐质量、(填序号)、称量精盐质量、计算。(2)、操作A中,用玻璃棒不断搅拌的目的是;操作B中用玻璃棒不断搅拌的目的是。(3)、称量精盐质量时,将所得精盐放置于托盘中的纸上,天平指针偏左,合理的操作是 。A、增加砝码或游码 B、增加药品 C、减少砝码或游码 D、减少药品(4)、若实验后发现产率偏低,可能的原因有 。A、滤纸破损 B、蒸发时有固体溅出 C、溶解时加入水不足量,部分盐没有溶解 D、将盐从蒸发皿转移到天平上称量时,没有转移干净33. 用下图所示装置测定空气中氧气的体积分数,实验时先在实际容积为250mL 的集气瓶中装进50mL的水,在粗铜丝末端的铜勺中放足量白磷,按图连好仪器,点燃酒精灯加热铜丝一端,白磷燃烧。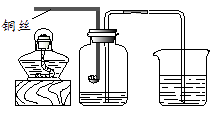 (1)、实验中主要利用铜的性。(2)、写出白磷燃烧反应的化学方程式。(3)、若实验成功,最终集气瓶中水的体积约为mL。(4)、白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是;由此现象分析,影响气体压强的主要因素有。34. 甲、乙两位同学分别用右图所示装置进行实验。
(1)、实验中主要利用铜的性。(2)、写出白磷燃烧反应的化学方程式。(3)、若实验成功,最终集气瓶中水的体积约为mL。(4)、白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是;由此现象分析,影响气体压强的主要因素有。34. 甲、乙两位同学分别用右图所示装置进行实验。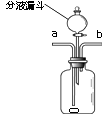 (1)、甲同学验证燃烧的条件。取一小块白磷放入广口瓶中,一段时间白磷没有燃烧,然后从分液漏斗中加入适量的 , 白磷仍然没有燃烧,再从a管通入 , 白磷发生燃烧,该实验证明可燃物燃烧需要与氧气接触、温度达到着火点这两个条件。
(1)、甲同学验证燃烧的条件。取一小块白磷放入广口瓶中,一段时间白磷没有燃烧,然后从分液漏斗中加入适量的 , 白磷仍然没有燃烧,再从a管通入 , 白磷发生燃烧,该实验证明可燃物燃烧需要与氧气接触、温度达到着火点这两个条件。
(2)、乙同学验证二氧化碳与水的反应。为验证使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是(填序号,可重复选用)。①从b端通氮气 ②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳 ④从分液漏斗中滴加适量水
三、实验探究题
-
35. 近几年我国某些城市酸雨污染较为严重,主要原因是燃烧含硫量高的煤及机动车排放的尾气。
【实验目的】验证煤中含有碳元素,检验是否含有硫元素
(1)、【查阅资料】①已知煤完全燃烧后,其中的碳和硫元素基本都转化成二氧化碳和二氧化硫。
②二氧化碳与高锰酸钾不反应。
③二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为:
5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2 X ,其中X的化学式是:。
④二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊,反应的化学方程式为:SO2+Ca(OH)2=CaSO3↓+H2O。
根据上述资料,甲、乙同学进行了如下实验探究。
(2)、【实验探究】甲同学进行了如下图所示A、B两个实验:
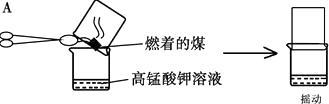
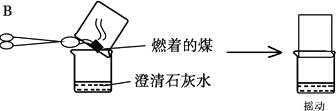
实验现象为 A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
由此甲同学认为:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
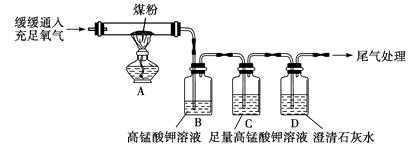
乙同学认为甲同学的方案不合理,于是进行了如下图所示实验(夹持装置略去):
【结论与反思】
①乙同学认为甲同学的实验方案不合理,其理由是:。
②上图C装置的作用是。
③要证明煤中含有碳元素和硫元素的现象是:。
四、简答题
-
36. 将6.8 g含杂质的锌粒加入到80 g过量的稀硫酸中(锌与稀硫酸反应的化学方程式:Zn+H2SO4=ZnSO4+H2↑;杂质不溶于水,也不与稀硫酸反应),充分反应后过滤,称得滤液质量为86.3 g。试计算:
(1)、反应生成氢气的质量;(2)、锌粒中所含锌的质量分数(精确到0.1%)。
-