江苏省苏州市工业园区2017-2018学年九年级上学期化学12月调研考试试卷
试卷日期:2017-12-29 考试类型:月考试卷
一、单项选择题
-
1. 下列属于物理变化的是( )A、干冰升华 B、煤燃烧 C、食物腐烂 D、铁丝生锈2. 人体中化学元素含量的多少,会直接影响人体的健康。下列人体所缺元素与健康关系表述错误的是( )A、缺铁会引起贫血 B、缺碘会引起龋齿 C、缺钙会引起老年人骨质疏松 D、缺锌会引起发育不良、智力低下3. 下列物质不属于金属材料的是( )A、不锈钢 B、氧化铁 C、黄金 D、硬铝4. 有关化学用语说法正确的是( )A、钙的元素符号Cu B、碳酸钠的化学式为NaCO3 C、2Fe2+表示2个铁离子 D、2H表示两个氢原子5. 燃煤时要特别注意室内通风,以免生成的有毒气体造成人员中毒。有毒气体主要指( )A、一氧化碳 B、氮气 C、氧气 D、二氧化碳6. 下列物质分散在水中能形成溶液的是( )A、泥土 B、面粉 C、高锰酸钾 D、食用油7. 金属材料在人类活动中已得到越来越广泛的应用.下列性质属于金属共性的是( )A、硬度很大、熔点很高 B、有良好的导电性、传热性 C、是银白色的固体 D、易与酸反应产生氢气8. 下列物质中很难导电的是( )A、蔗糖溶液 B、铜 C、石墨 D、氯化钠溶液9. 交警常用装有重铬酸钾(K2Cr2O7)的仪器检测司机是否酒后驾车,因为酒中的乙醇分子能使橙红色的重铬酸钾变成绿色的硫酸铬[Cr2(SO4)3].重铬酸钾和硫酸铬中铬元素的化合价依次是( )
A、+6 +3 B、+3 +3 C、+3 +5 D、+3 +610. 有关微观粒子的说法,错误的是( )
A、分子、原子、离子都是构成物质的微粒 B、分子是由原子构成的 C、氯化钠是由氯化钠分子构成的 D、保持水的化学性质的最小微粒是水分子11. 下列处理事故的说法错误的是( )A、厨房管道煤气泄漏,立即关闭阀门并开窗通风 B、电器着火应先切断电源,再用液态二氧化碳灭火器扑灭 C、扑灭森林火灾的有效方法之一是将大火蔓延路线前的一片树木砍掉 D、房屋失火,可使用大量的冷却剂(如水、干冰等),降低可燃物的着火点12. 生活中的下列现象,用分子的相关知识解释不正确的是( )A、湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关 B、一滴水中大约有1.67×1021个水分子,说明分子的体积和质量很小 C、水沸腾时,掀起壶盖,说明分子大小随温度升高而增大 D、1L黄豆和1L芝麻混合,体积小于2L,不能说明分子之间有间隙13. 下列说法中正确的是( )A、合金中一定不含有非金属 B、生铁可以完全溶解在足量的稀盐酸中 C、不锈钢是永不生锈的钢铁 D、高炉炼铁的废气必须要经过处理才能排放到大气中14. 下列是几种微粒的结构示意图,有关说法错误的是( )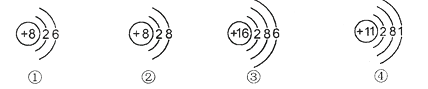 A、①和②属于同种元素 B、②表示的微粒符号为O2- C、①和③的化学性质相似 D、④表示的原子具有稳定结构15. 下列有关铁反应的实验现象的描述错误的是( )A、铁丝在氧气中燃烧,火星四射,生成黑色固体 B、铁丝置于稀硫酸中,表面产生气泡,溶液逐渐由无色变成蓝色 C、在潮湿的空气中,铁钉表面逐渐产生疏松的红棕色固体 D、铁钉浸没在硫酸铜溶液中,表面覆盖了一层红色物质16. 下列关于溶液的说法中,正确的是( )A、溶液都是无色透明的 B、凡是均一的、稳定的液体都是溶液 C、蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度 D、氢氧化钠溶液能导电,因为溶液中有较多自由移动的离子17. 下图是探究铁制品锈蚀条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得出的结论错误的是( )
A、①和②属于同种元素 B、②表示的微粒符号为O2- C、①和③的化学性质相似 D、④表示的原子具有稳定结构15. 下列有关铁反应的实验现象的描述错误的是( )A、铁丝在氧气中燃烧,火星四射,生成黑色固体 B、铁丝置于稀硫酸中,表面产生气泡,溶液逐渐由无色变成蓝色 C、在潮湿的空气中,铁钉表面逐渐产生疏松的红棕色固体 D、铁钉浸没在硫酸铜溶液中,表面覆盖了一层红色物质16. 下列关于溶液的说法中,正确的是( )A、溶液都是无色透明的 B、凡是均一的、稳定的液体都是溶液 C、蔗糖溶液上半部分溶液的甜度低于下半部分溶液的甜度 D、氢氧化钠溶液能导电,因为溶液中有较多自由移动的离子17. 下图是探究铁制品锈蚀条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得出的结论错误的是( )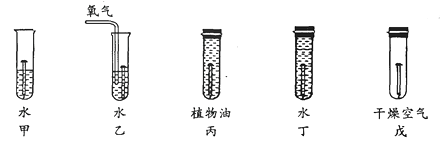 A、甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊 B、丙中的铁钉不生锈 C、铁生锈的主要条件是与空气、水直接接触 D、丁中铁钉生锈最严重18. 最近“纸火锅”(如图)逐渐流行起来。“纸火锅”是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧。对此现象,下列解释合理的是( )
A、甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊 B、丙中的铁钉不生锈 C、铁生锈的主要条件是与空气、水直接接触 D、丁中铁钉生锈最严重18. 最近“纸火锅”(如图)逐渐流行起来。“纸火锅”是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧。对此现象,下列解释合理的是( ) A、纸张不是可燃物,不能燃烧 B、纸张被水浸湿,导致着火点降低 C、水蒸发时吸热,温度达不到纸张的着火点 D、空气不充足,纸张不会燃烧19. 下列有关化学知识的描述正确的是( )A、催化剂不仅能改变化学反应速率,而且会增加生成物的质量 B、金属都能与酸溶液反应,而且反应的剧烈程度能体现金属活动性的强弱 C、由同种元素组成的物质一定是单质 D、合金的性能一般优于纯金属20. 对下面一些现象和事实的解释错误的是( )A、用活性炭去除冰箱中的异味——活性炭具有吸附性 B、水在高温条件下能分解得到氢气和氧气——水是由氢元素和氧元素组成的 C、铝质饭盒不宜贮存酸性食品——铝易与酸性溶液反应 D、用醋酸浸过的铁钉很易锈蚀——醋酸对铁钉锈蚀起到催化作用21. 下列说法错误的是( )A、煮沸的汤比煮沸的水温度高 B、在积雪的公路上撒盐可加快冰雪融化 C、可用水区分NaOH固体和NH4NO3固体 D、用洗涤剂除油污是因为洗涤剂能将油污溶解,形成溶液22. 甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如下所示:
A、纸张不是可燃物,不能燃烧 B、纸张被水浸湿,导致着火点降低 C、水蒸发时吸热,温度达不到纸张的着火点 D、空气不充足,纸张不会燃烧19. 下列有关化学知识的描述正确的是( )A、催化剂不仅能改变化学反应速率,而且会增加生成物的质量 B、金属都能与酸溶液反应,而且反应的剧烈程度能体现金属活动性的强弱 C、由同种元素组成的物质一定是单质 D、合金的性能一般优于纯金属20. 对下面一些现象和事实的解释错误的是( )A、用活性炭去除冰箱中的异味——活性炭具有吸附性 B、水在高温条件下能分解得到氢气和氧气——水是由氢元素和氧元素组成的 C、铝质饭盒不宜贮存酸性食品——铝易与酸性溶液反应 D、用醋酸浸过的铁钉很易锈蚀——醋酸对铁钉锈蚀起到催化作用21. 下列说法错误的是( )A、煮沸的汤比煮沸的水温度高 B、在积雪的公路上撒盐可加快冰雪融化 C、可用水区分NaOH固体和NH4NO3固体 D、用洗涤剂除油污是因为洗涤剂能将油污溶解,形成溶液22. 甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如下所示: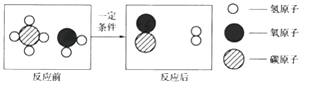
根据以上微观示意图得出的结论正确的是( )
A、反应前后各元素的化合价均不变 B、化学方程式中甲烷和水的化学计量数之比为1:1 C、该反应中含氢元素的化合物有3种 D、水煤气的成分是一氧化碳和氧气23. 实验室用大理石和稀盐酸反应制备CO2 . 下列装置(省略了夹持仪器)中属于能用于制备CO2的发生装置,且能随时控制反应的发生与停止的是( )A、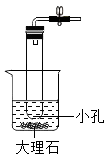 B、
B、 C、
C、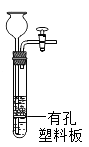 D、
D、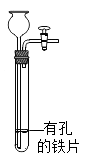 24. 某化合物在4.8g氧气中完全燃烧,生成4.4g二氧化碳和2.7g水.关于该物质的推断不正确的是( )A、该化合物为2.3g B、该化合物一定含碳、氢、氧元素 C、碳、氢元素质量比为4:1 D、分子中C,H原子个数比为1:225. 按要求填空。
24. 某化合物在4.8g氧气中完全燃烧,生成4.4g二氧化碳和2.7g水.关于该物质的推断不正确的是( )A、该化合物为2.3g B、该化合物一定含碳、氢、氧元素 C、碳、氢元素质量比为4:1 D、分子中C,H原子个数比为1:225. 按要求填空。
(1)、各种物质之间存在着某种联系。请分别选用“>”、“<”、“=”填写空白。
①空气中成分体积分数:氧气氮气;②核外电子数:钠离子钠原子;
③ 金属与稀盐酸反应的剧烈程度:锌片铁片;
④铜丝在火焰上灼烧,灼烧后的“铜丝”质量原铜丝的质量;
⑤硬铝,其硬度铝的硬度。
(2)、写出下列物质的名称①FeCl2; ②(NH4)2SO4; ③HNO3。
26. 完成下列化学方程式,并回答有关问题。(1)、水通电分解;正负极产生的气体的质量比为。(2)、常温下铝和氧气发生反应:;其基本反应类型是:反应。(3)、炼铁高炉内焦炭与二氧化碳反应:;该反应属于(选填“放热”或“吸热”)反应。(4)、碱式碳酸铜受热分解;(5)、久置的石灰水瓶壁形成一层白膜;(6)、实验室用锌和稀硫酸反应制氢气;其基本反应类型是:反应。27. 科学家最近在-100℃的低温下合成了一种化合物X,此分子的模型如图所示,其中每个 代表一个碳原子,每个
代表一个碳原子,每个  代表一个氢原子。
代表一个氢原子。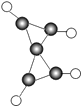 (1)、该分子的分子式为。(2)、该分子中碳原子和氢原子的质量之比为。
(1)、该分子的分子式为。(2)、该分子中碳原子和氢原子的质量之比为。
(3)、该分子中碳元素的质量分数为。
(4)、请补充该物质燃烧的化学方程式:+6O2 5CO2+。(5)、等质量的该物质与甲烷相比,燃烧时消耗的氧气量较(填“多”或“少”)。
28. 化学兴趣小组在实验室进行关于气体的实验,所用的部分装置如下图所示。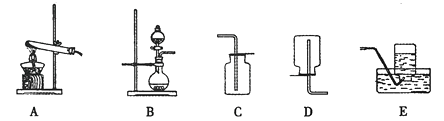 (1)、用B装置制取氧气,发生反应的化学方程式:。(2)、小张同学想探究二氧化碳能否用排水法收集,查了有关数据得知,常压常温下,1体积水中溶解二氧化碳为0.88体积(溶解数量有限);又实验如下,用排水法和排空气法各收集一试管二氧化碳,并倒置于氢氧化钠溶液中(资料:氢氧化钠溶液能吸收二氧化碳),发现用排水法收集二氧化碳的试管中气体全部被吸收,而用排空气法收集的气体只被吸收一半,由此得出结论:二氧化碳能否用排水法收集(填能或不能),用排水法收集二氧化碳的优点是。(3)、小李同学研究了木条复燃与氧气体积分数的关系,发现氧气占49%以上就能使带火星的木条复燃。右图F是他其中一次实验的装置,集气瓶中
(1)、用B装置制取氧气,发生反应的化学方程式:。(2)、小张同学想探究二氧化碳能否用排水法收集,查了有关数据得知,常压常温下,1体积水中溶解二氧化碳为0.88体积(溶解数量有限);又实验如下,用排水法和排空气法各收集一试管二氧化碳,并倒置于氢氧化钠溶液中(资料:氢氧化钠溶液能吸收二氧化碳),发现用排水法收集二氧化碳的试管中气体全部被吸收,而用排空气法收集的气体只被吸收一半,由此得出结论:二氧化碳能否用排水法收集(填能或不能),用排水法收集二氧化碳的优点是。(3)、小李同学研究了木条复燃与氧气体积分数的关系,发现氧气占49%以上就能使带火星的木条复燃。右图F是他其中一次实验的装置,集气瓶中有约占总体积40%水,氧气从(填“a”或“b”)导管口进入,排尽集气瓶中的水,收集氧气后集气瓶中氧气的体积分数是。
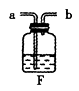 (4)、右图G装置也可制取氢气。G装置的优点是可随时控制反应的发生和停止。若打开活塞,固体与液体接触,反应便能发生,请简述使G装置中反应停止的操作为:。
(4)、右图G装置也可制取氢气。G装置的优点是可随时控制反应的发生和停止。若打开活塞,固体与液体接触,反应便能发生,请简述使G装置中反应停止的操作为:。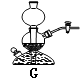 29. 甲图是一氧化碳与氧化铁反应装置的示意图,乙图是高炉练铁示意图。请回答下列问题。
29. 甲图是一氧化碳与氧化铁反应装置的示意图,乙图是高炉练铁示意图。请回答下列问题。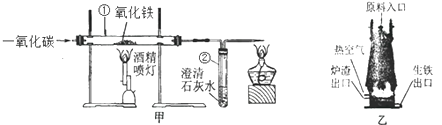 (1)、写出甲图硬质玻璃管内反应的化学方程式:。(2)、实验过程中仪器①的现象是 , 仪器②中的现象是。
(1)、写出甲图硬质玻璃管内反应的化学方程式:。(2)、实验过程中仪器①的现象是 , 仪器②中的现象是。
(3)、图乙是工业生产中炼铁高炉的结构图.实际生产中炼铁的原料铁矿石、焦炭、石灰石是从原料入口加入的,其中焦炭在高炉炼铁时的作用之一是 , 另一作用为生成一氧化碳。生铁出口低于炉渣出口的原因是。
(4)、现代设计高炉的高度可达70米,其优点是。
30. 某工厂在生产过程中会产生大量氧化铜废料(杂质与稀硫酸不发生反应且不溶于水),工厂技术科设计如下的生产流程来回收金属,其流程图如下: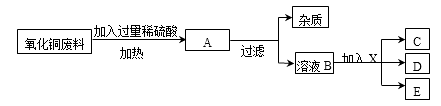
试回答下列有关问题:
(1)、在加热条件下,氧化铜能与稀硫酸迅速反应生成硫酸铜和一种氧化物,该氧化物是相对分子质量最小的氧化物。则氧化铜与稀硫酸反应的化学方程式为;(2)、过滤时用到的玻璃仪器有玻璃棒、烧杯和;(3)、溶液B中的溶质为:;(4)、若D是一种浅绿色溶液,C是一种最轻的气体,则X的化学式为 , 在溶液B中加入X时发生的化学反应方程式为31. 两化学兴趣小组测定某石灰石样品中碳酸钙的质量分数(假定:石灰石样品中除碳酸钙外,其余物质不与稀盐酸反应也不溶于水;且为了反应充分,尽可能的将石灰石样品粉碎).不同的小组采用了不同的方法,但是他们都成功的测定了所取样品中碳酸钙的质量分数.(1)、【第一组】①称取12g样品放入烧杯;
②加入足量的稀盐酸至不再产生气体时,过滤、洗涤、干燥后称量剩余固体质量为3.6g;
③根据剩余固体的质量求出样品中碳酸钙的质量分数为。
(2)、【第二组】①称取6g样品:按规范操作,用托盘天平称取6g样品时,若指针略向左偏转,要使指针居中的恰当操作是:;把称取好的样品放入烧杯中(烧杯质量为10g).
②将50g稀盐酸分5次加入,每次加入稀盐酸后,用玻璃棒不断搅拌,搅拌的目的是 , 然后对烧杯(包括溶液和残余固体)进行了称量,记录如下表:
第1次
第2次
第3次
第4次
第5次
加入稀盐酸的总质量(g)
10
20
30
40
50
烧杯和药品总质量(g)
25.56
35.12
44.68
54.24
64.24
(3)、分析数据,进行计算①样品完全反应后生成二氧化碳的质量为g.
②石灰石样品中碳酸钙的质量分数是多少?(计算结果精确到0.1 %)
③最后所得溶液的质量为g.