2023年上海市金山区中考一模化学试题
试卷日期:2023-03-05 考试类型:中考模拟
一、选择题(本大题共17题,1-14每题有一个正确选项,15-17每题有1-2个正确选项)
-
1. 常温下测得一些食物的近似 pH,酸性最强的是( )A、苹果汁~3.1 B、番茄汁~4.2 C、牛奶~6.5 D、玉米粥~7.52. 物质的组成中含有原子团的是A、NaCl B、KNO3 C、CO2 D、Fe2O33. 空气中体积分数约占78%的气体是( )A、二氧化碳 B、氮气 C、氧气 D、稀有气体4. 自来水生产中,能起到杀菌消毒作用的是A、活性炭 B、氯气 C、明矾 D、氯化铁5. 具有良好发展前景的绿色能源是A、氢气 B、木炭 C、天然气 D、石油6. 属于溶液的是A、泥水 B、牛奶 C、石灰浆 D、矿泉水7. 属于同素异形体的一组物质是A、水与双氧水 B、金刚石与石墨 C、液氧与氧气 D、冰与干冰8. 在氧气中燃烧,产生明亮蓝紫色火焰的是()A、硫 B、红磷 C、铁丝 D、氢气9. 能使气体溶解度增大的操作是A、增大压强 B、升高温度 C、增加溶剂 D、振荡溶液10. 物质的用途只体现其物理性质的是A、N2:作保护气 B、CO:冶炼金属 C、O2:供给呼吸 D、稀有气体:作电光源11. 能使燃料充分燃烧的措施是A、充分利用反应的余热 B、减少空气通入量 C、把固体燃料粉碎 D、净化尾气12. 关于分子和原子的说法正确的是A、分子比原子大 B、原子在化学变化中可以再分 C、分子或原子都可以构成物质 D、分子是保持物质性质的一种微粒13. 关于H2O2的说法,正确的是A、氢、氧元素的质量比为1:1 B、过氧化氢由氢元素和氧元素组成 C、摩尔质量为34g D、过氧化氢由氢分子和氧分子构成14. 只含有碳酸钙和氧化钙的混合物,测得其中钙元素的质量分数为50%。取该混合物32g充分煅烧后将剩余固体投入水中,充分反应后生成氢氧化钙的质量为A、7.4g B、14.8g C、29.6g D、37g15. 某实验小组用下图装置探究二氧化碳的性质,说法正确的是
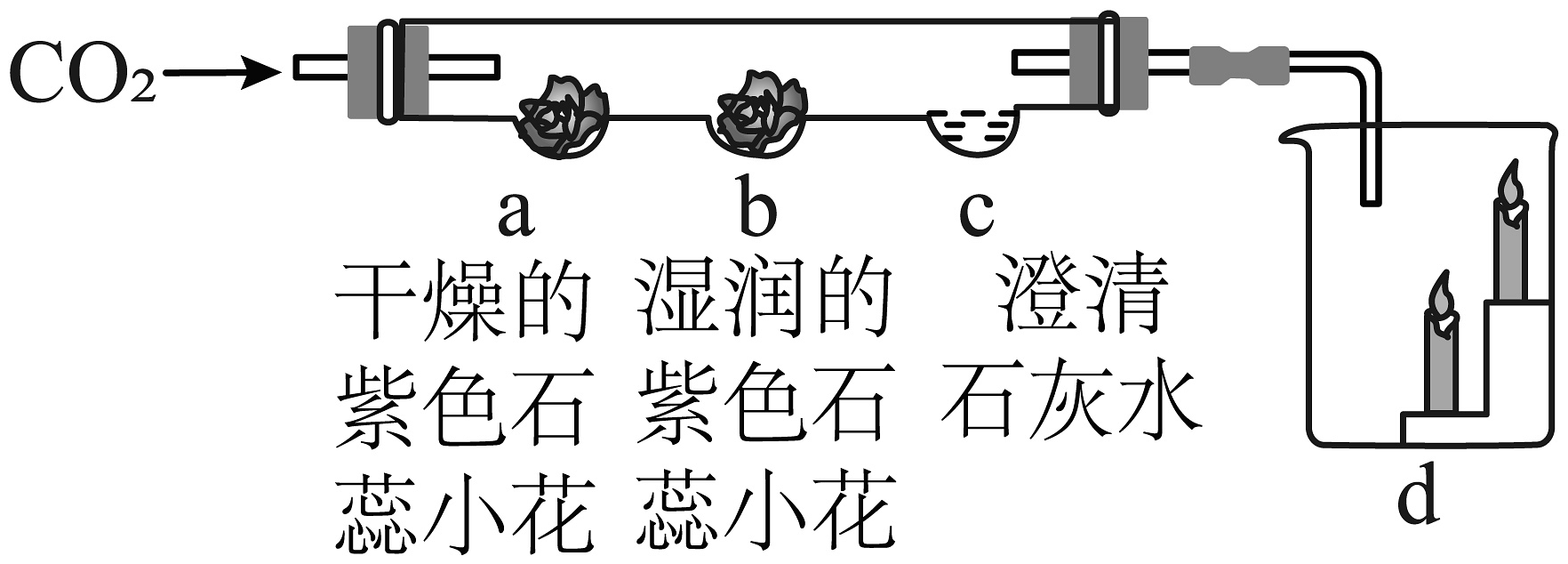 A、a处小花不变色,b小花变蓝色 B、c处澄清石灰水变浑浊 C、该装置不涉及二氧化碳的物理性质 D、该装置具有一次性完成多个实验的优点16. 如图示某化学反应前后的微观示意图,说法正确的是
A、a处小花不变色,b小花变蓝色 B、c处澄清石灰水变浑浊 C、该装置不涉及二氧化碳的物理性质 D、该装置具有一次性完成多个实验的优点16. 如图示某化学反应前后的微观示意图,说法正确的是 A、参加反应的两种分子个数比为1:1 B、生成物有3种 C、生成物全部是化合物 D、反应前后元素的化合价不变17. 化学概念之间具有并列、包含、交叉等关系,如图表示M、N之间的包含关系。下表中符合图示关系的是
A、参加反应的两种分子个数比为1:1 B、生成物有3种 C、生成物全部是化合物 D、反应前后元素的化合价不变17. 化学概念之间具有并列、包含、交叉等关系,如图表示M、N之间的包含关系。下表中符合图示关系的是
选项
M
N
A
单质
纯净物
B
含氧化合物
氧化物
C
纯净物
混合物
D
纯净物
化合物
A、A B、B C、C D、D二、简答题(本大题共4分,共30分)
-
18. 北京时间2021年12月9日,“天宫课堂”第一课在中国空间站正式开讲并直播。(1)、王亚平老师在失重环境下将泡腾片放入一蓝色水球中,泡腾片不断产生气泡,却始终不会离开水球,水球逐渐变成了“气泡球”。泡腾片中维生素C(C6H8O6)由种元素组成,其中C、H原子个数比为 , 1mol C6H8O6约含有个O原子。(2)、王亚平老师变出奥运五环的实验中,溴百里酚蓝的“蓝色”与甲基橙的“黄色”都利用了Na2CO3溶液呈(填“酸性”或“碱性”)的性质。第二环利用碘化钾与碘酸钾反应生成碘单质,碘单质遇淀粉变深蓝色。碘酸钾(KIO3)中碘元素的化合价为。(3)、天宫空间站通过电解水为宇航员供氧,如图为实验室模拟电解水的装置。该反应的化学方程式是 , 其中收集到氧气的试管是(填“a”或“b”)。空间站内,用宇航员呼出的二氧化碳和电解水生成的氢气,在一定条件下反应生成水和甲烷,该过程属于(填“物理”或“化学”)变化,水中氧元素以(填“游离”或“化合”)态存在。
 19. 下图是实验室制取气体的部分装置,请回答下列问题。
19. 下图是实验室制取气体的部分装置,请回答下列问题。 (1)、用氯酸钾和二氧化锰共热制备氧气的化学方程式是 , 该反应的基本类型是 , 二氧化锰的作用是。若要制取0.06mol氧气,至少需要g氯酸钾参加反应。(2)、用双氧水和二氧化锰制备氧气,为使反应平稳进行,应选用的发生装置是(填编号);为了收集纯净的氧气,应选用的收集装置是(填编号)。(3)、用块状大理石和稀盐酸制备二氧化碳,控制所加稀盐酸的量,反应时丙装置内液面位于(填“a”、“b”或“c”)处为宜,用戊装置收集二氧化碳的验满方法是。不用粉末状大理石制备二氧化碳的原因是。20. NaCl、KNO3的部分溶解度数据见下表。
(1)、用氯酸钾和二氧化锰共热制备氧气的化学方程式是 , 该反应的基本类型是 , 二氧化锰的作用是。若要制取0.06mol氧气,至少需要g氯酸钾参加反应。(2)、用双氧水和二氧化锰制备氧气,为使反应平稳进行,应选用的发生装置是(填编号);为了收集纯净的氧气,应选用的收集装置是(填编号)。(3)、用块状大理石和稀盐酸制备二氧化碳,控制所加稀盐酸的量,反应时丙装置内液面位于(填“a”、“b”或“c”)处为宜,用戊装置收集二氧化碳的验满方法是。不用粉末状大理石制备二氧化碳的原因是。20. NaCl、KNO3的部分溶解度数据见下表。温度
10
20
40
60
80
100
溶解度
(g/100g水)
KNO3
20.9
31.6
63.9
110
169
246
NaCl
35.8
36
36.6
37.3
38.4
39.8
(1)、20℃时,NaCl的溶解度是g/100g水,该温度下NaCl饱和溶液的溶质质量分数是;若要将NaCl饱和溶液转化为不饱和溶液,可采取的方法是(写出一种即可)。(2)、20℃时,将30g硝酸钾加入到50g水中充分溶解,所得溶液是(填“饱和”或“不饱和”溶液)。(3)、当温度在范围内时,可以配制溶质质量分数相等的KNO3和NaCl的饱和溶液。(4)、某NaCl样品中混有少量KNO3 , 可利用溶解度差异进行提纯。称取52g样品进行如下实验:
样品中氯化钠的质量是g。若步骤III中温度降低到40℃时过滤,将不能得到纯净的氯化钠晶体,请结合相关数据分析说明。
21. 某学习小组为验证碳及其化合物的性质设计如下图所示的实验装置进行实验。 (1)、甲处玻璃管中木炭和二氧化碳在高温条件下生成一氧化碳,该反应中木炭表现出(填“氧化性”或“还原性”)。(2)、乙处玻璃管中的实验现象是 , 发生反应的化学方程式是。(3)、丙装置的作用是。(4)、丁处石灰水变浑浊,能否检验乙处反应生成的二氧化碳?请说明理由。
(1)、甲处玻璃管中木炭和二氧化碳在高温条件下生成一氧化碳,该反应中木炭表现出(填“氧化性”或“还原性”)。(2)、乙处玻璃管中的实验现象是 , 发生反应的化学方程式是。(3)、丙装置的作用是。(4)、丁处石灰水变浑浊,能否检验乙处反应生成的二氧化碳?请说明理由。