2022年中考化学二轮专题复习-分子、原子、离子和元素
试卷日期:2022-03-29 考试类型:二轮复习
一、单选题
-
1. 下列物质由分子构成的是( )A、汞 B、氨气 C、氯化钠 D、金刚石2. 元素观是化学的重要观念之一。下列有关元素的说法错误的是( )A、物质是由元素组成的 B、同种元素的原子核内中子数相同 C、在化学变化中元素的种类不发生改变 D、元素周期表中原子序数等于该元素原子核内的质子数3. 下列结构示意图表示元素周期表中同一纵行的原子的是( )
 A、①② B、②③ C、①③ D、①④4. 将100 mL水与100 mL酒精混合,所得溶液体积小于200 mL。下列对此现象的解释最合理的是( )A、分子是由原子构成的 B、分子的质量和体积都是很小的 C、分子是不断运动的 D、分子间是有间隔的5. 对于图示
A、①② B、②③ C、①③ D、①④4. 将100 mL水与100 mL酒精混合,所得溶液体积小于200 mL。下列对此现象的解释最合理的是( )A、分子是由原子构成的 B、分子的质量和体积都是很小的 C、分子是不断运动的 D、分子间是有间隔的5. 对于图示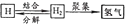 理解错误的是( ) A、原子可结合成分子 B、可用
理解错误的是( ) A、原子可结合成分子 B、可用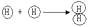 表示氢分子的形成过程
C、物质都由分子构成
D、化学变化的基础是分子的破裂和原子的重新组合
6. 生活中会听到这样的说法“缺铁会贫血”、“用铁锅做菜会补铁”。这里所说的“铁”是指( )
表示氢分子的形成过程
C、物质都由分子构成
D、化学变化的基础是分子的破裂和原子的重新组合
6. 生活中会听到这样的说法“缺铁会贫血”、“用铁锅做菜会补铁”。这里所说的“铁”是指( )
A、铁原子 B、铁元素 C、铁单质 D、碎铁屑7. 用分子的观点对下列常见现象的解释,错误的是( )A、热胀冷缩﹣﹣分子大小随温度变化而变化 B、花香四溢﹣﹣分子不停地运动 C、压缩气体﹣﹣分子之间间隔减小 D、过氧化氢分解﹣﹣分子发生了变化8. 下列化学用语错误的是( )A、2个氢原子:2H B、铝离子:Al3+ C、S2-的结构示意图: D、氧化铁:Fe2O3
9. 原子失去最外层电子或最外层得到电子后,一定不会引起改变的是( )
D、氧化铁:Fe2O3
9. 原子失去最外层电子或最外层得到电子后,一定不会引起改变的是( )①化学性质 ②粒子的电性 ③原子核 ④电子层数 ⑤最外层电子数 ⑥核外电子总数
A、②④⑤ B、③④⑥ C、③ D、①③⑤⑥10. 甲醛是装修材料中常见的污染物.其分子结构如图所示,下列说法正确的是( )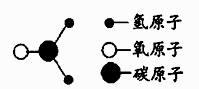 A、甲醛由碳、氢、氧三种元素组成 B、甲醛的相对分子质量为30g C、甲醛由一个碳原子、1个氢分子和1个氧原子构成 D、甲醛中碳、氢、氧三种元素的质量比为1:2:111. 下列相对分子质量的计算不正确的是( )A、P2O5:31×2+16×5=142 B、2H2O:2×2×1+16=20 C、2CO2:2×(12+16×2)=88 D、CaCO3:40+12+16×3=10012. 下列化合物中含有两种不同原子团的是( )
A、甲醛由碳、氢、氧三种元素组成 B、甲醛的相对分子质量为30g C、甲醛由一个碳原子、1个氢分子和1个氧原子构成 D、甲醛中碳、氢、氧三种元素的质量比为1:2:111. 下列相对分子质量的计算不正确的是( )A、P2O5:31×2+16×5=142 B、2H2O:2×2×1+16=20 C、2CO2:2×(12+16×2)=88 D、CaCO3:40+12+16×3=10012. 下列化合物中含有两种不同原子团的是( )
A、NH4NO3 B、NH4Cl C、H2SO4 D、Cu(OH)213. 以下事例主要体现分子间的间隔改变的是( )
A、 B、
B、 C、
C、 D、
D、 14. 构成药物吗丁啉的分子中含有22个碳原子、24个氢原子、5个氮原子、2个氧原子、1个氯原子。由此可知构成吗叮啉的元素种类是( )A、54种 B、1种 C、5种 D、24种15. 已知一个碳 原子的质量为m kg,一个R原子的质量为n kg,则R原子的相对原子质量的表达式为A、 B、 C、 D、16. M元素原子的核电荷数为a,它的阳离子 与N元素的阴离子 核外电子排布相同,则N元素原子核内质子数为A、 B、 C、 D、17. Fe、H表示的意义分别是( )A、Fe表示铁元素、H表示氢元素 B、Fe表示1个铁原子、H表示1个氢原子 C、Fe表示铁元素,也表示1个铁原子;H表示氢元素,也表示1个氢原子 D、Fe表示铁元素,也表示1个铁原子,还表示单质铁;H表示氢元素,也表示1个氢原子18. 下列各组元素,都属于非金属元素的是( )A、溴、汞、碳 B、氧、氢、镁 C、磷、碘、氟 D、氯、钙、锰19. 下列关于离子的说法不正确的是( )A、离子都带电荷,所以带电荷的微粒一定是离子 B、原子失去电子形成阳离子,得到电子形成阴离子 C、原子形成离子后,原子核内质子数不发生变化 D、带电荷的原子和原子团都称为离子20. 某元素的微粒37X﹣的核外电子数为18,则该元素原子的中子数是( )A、17 B、18 C、19 D、20
14. 构成药物吗丁啉的分子中含有22个碳原子、24个氢原子、5个氮原子、2个氧原子、1个氯原子。由此可知构成吗叮啉的元素种类是( )A、54种 B、1种 C、5种 D、24种15. 已知一个碳 原子的质量为m kg,一个R原子的质量为n kg,则R原子的相对原子质量的表达式为A、 B、 C、 D、16. M元素原子的核电荷数为a,它的阳离子 与N元素的阴离子 核外电子排布相同,则N元素原子核内质子数为A、 B、 C、 D、17. Fe、H表示的意义分别是( )A、Fe表示铁元素、H表示氢元素 B、Fe表示1个铁原子、H表示1个氢原子 C、Fe表示铁元素,也表示1个铁原子;H表示氢元素,也表示1个氢原子 D、Fe表示铁元素,也表示1个铁原子,还表示单质铁;H表示氢元素,也表示1个氢原子18. 下列各组元素,都属于非金属元素的是( )A、溴、汞、碳 B、氧、氢、镁 C、磷、碘、氟 D、氯、钙、锰19. 下列关于离子的说法不正确的是( )A、离子都带电荷,所以带电荷的微粒一定是离子 B、原子失去电子形成阳离子,得到电子形成阴离子 C、原子形成离子后,原子核内质子数不发生变化 D、带电荷的原子和原子团都称为离子20. 某元素的微粒37X﹣的核外电子数为18,则该元素原子的中子数是( )A、17 B、18 C、19 D、20二、填空题
-
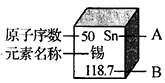
21. 元素周期表是学习化学的重要工具,下图是表中的一格,其中A表示;B表示。
 22. 计算下列物质的相对分子质量。
22. 计算下列物质的相对分子质量。氨气(NH3):; 氧气(O2):; 高锰酸钾(KMnO4):; 葡萄糖(C6H12O6):。
23. M元素的离子为M2+ , 其核外电子数为a,核内中子数为b,则M的相对原子质量为 .24. R原子相对原子质量为a,R2﹣核外电子数为b,则R原子的中子数为 . 如图微粒结构示意图中,化学性质相似的是 , 属于同种元素的是 .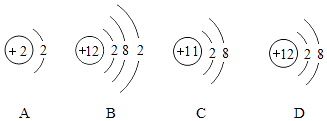 25. 月球上含有丰富的核聚变燃料“氦﹣3(3He)”,已知“碳﹣13(13C)”是指原子核内含有六个质子、7个中子的碳原子,则“3He”所指的氦原子,核内含有个质子、个中子.26. 已知两种离子A2+和B2﹣的核外电子数相同,其中B原子的质子数为a,则A原子的质子数为 .27. 居里夫人在1898年从铀盐废料中提炼出镭.镭是具有放射性,会裂变成一个质子数为86,中子数为136的氡原子和一个具有2个质子和2个中子的氦原子,并放出热量,则镭原子的质子数为 , 相对原子质量为 .28. 从“分子、原子、质子、中子、电子、原子核、阳离子、阴离子”中,选出所有适合的微粒名称填写下列空白.
25. 月球上含有丰富的核聚变燃料“氦﹣3(3He)”,已知“碳﹣13(13C)”是指原子核内含有六个质子、7个中子的碳原子,则“3He”所指的氦原子,核内含有个质子、个中子.26. 已知两种离子A2+和B2﹣的核外电子数相同,其中B原子的质子数为a,则A原子的质子数为 .27. 居里夫人在1898年从铀盐废料中提炼出镭.镭是具有放射性,会裂变成一个质子数为86,中子数为136的氡原子和一个具有2个质子和2个中子的氦原子,并放出热量,则镭原子的质子数为 , 相对原子质量为 .28. 从“分子、原子、质子、中子、电子、原子核、阳离子、阴离子”中,选出所有适合的微粒名称填写下列空白.①在化学变化中,一定发生变化的微粒是 .
②带正电荷的是 .
③一般来说,同一种原子里,数目一定相等的是 .
④构成原子的微粒有
29. 请你根据学习的化学知识回答下列问题: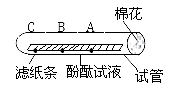
浓氨水可以使酚酞试液变成红色,它具有挥发性 往如图试管口的棉花滴浓氨水,再往滤纸条上从右往左依次滴上A、B、C三滴酚酞试液,可观察到的现象是 ;此现象说明分子具有 的性质。
30. 小丽为探究分子的运动速率与温度的关系:取等量的品红分别加入等量的热水和冷水中,观察并记录实验现象在下表中:实验过程
冷水
热水
开始
红色扩散较慢
红色扩散很快
长久放置
最终均成为红色、均匀、透明的液体
根据实验现象,可得出结论:。
三、综合题
-
31. 广西矿产资源丰富,铟的生产规模居世界同类企业首位。图1是元素周期表中铟元素的信息,图2是铟原子的结构示意图,回答下列问题:
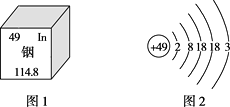 (1)、铟元素属于元素,其原子核外共有个电子层。(2)、在化学反应中,铟原子容易电子形成铟离子,铟离子的化学符号为。(3)、画出第13号元素的原子结构示意图 , 该元素与铟元素在元素周期表中处于同一个(填“周期”或“族”)。32. 元素周期表是学习和研究化学的重要工具,请分析下图中的信息并回答下列问题。
(1)、铟元素属于元素,其原子核外共有个电子层。(2)、在化学反应中,铟原子容易电子形成铟离子,铟离子的化学符号为。(3)、画出第13号元素的原子结构示意图 , 该元素与铟元素在元素周期表中处于同一个(填“周期”或“族”)。32. 元素周期表是学习和研究化学的重要工具,请分析下图中的信息并回答下列问题。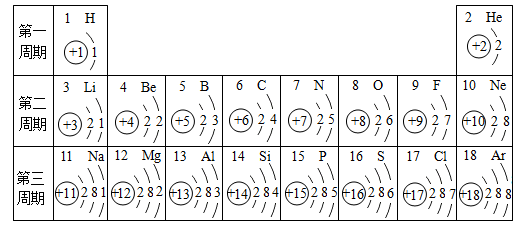 (1)、原子序数为3的元素属于(填“金属”或“非金属”)元素。(2)、氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的相同。(3)、在化学反应中,原子序数为17的元素的原子容易(填“得到”或“失去”)电子。(4)、由原子序数为11、17的两种元素组成物质的化学式是 , 该物质是由(填分子、原子或离子)构成。33. 元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~18号元素的原子结构示意图,请回答下列问题。
(1)、原子序数为3的元素属于(填“金属”或“非金属”)元素。(2)、氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的相同。(3)、在化学反应中,原子序数为17的元素的原子容易(填“得到”或“失去”)电子。(4)、由原子序数为11、17的两种元素组成物质的化学式是 , 该物质是由(填分子、原子或离子)构成。33. 元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~18号元素的原子结构示意图,请回答下列问题。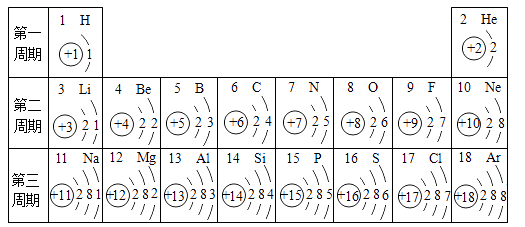 (1)、原子序数为13的元素的原子失去电子后的离子符号是。(2)、如图表示碘原子的结构示意图,由图可知,碘元素应位于元素周期表中的第周期。
(1)、原子序数为13的元素的原子失去电子后的离子符号是。(2)、如图表示碘原子的结构示意图,由图可知,碘元素应位于元素周期表中的第周期。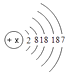 34. 下图是元素周期表中1~18号元素的相关信息,请认真分析并回答下列问题。
34. 下图是元素周期表中1~18号元素的相关信息,请认真分析并回答下列问题。 (1)、元素周期表是学习和研究化学的重要工具。俄国的化学家发现了元素周期律并编制出元素周期表。(2)、原子序数为5的元素的名称是 , 它位于元素周期表中第周期。(3)、在化学反应中,原子序数为16的元素的原子容易(填“得到”或“失去”)电子,所形成的粒子的符号是。(4)、如图是溴元素(Br)的原子结构示意图,那么,其中n为 , 分析氟原子和溴原子的结构示意图分析,可以发现:由于氟原子和溴原子的相同,所以它们的化学性质相似;
(1)、元素周期表是学习和研究化学的重要工具。俄国的化学家发现了元素周期律并编制出元素周期表。(2)、原子序数为5的元素的名称是 , 它位于元素周期表中第周期。(3)、在化学反应中,原子序数为16的元素的原子容易(填“得到”或“失去”)电子,所形成的粒子的符号是。(4)、如图是溴元素(Br)的原子结构示意图,那么,其中n为 , 分析氟原子和溴原子的结构示意图分析,可以发现:由于氟原子和溴原子的相同,所以它们的化学性质相似;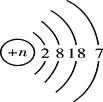 (5)、对1-18号元素的原子结构示意图进行分析,可以发现许多规律,如在同一周期,从左到右,核外电子数依次递增。请再总结出其它规律,并写出其中一条:。35. 资料一:据报道,浙西北藏着个聚宝盆,4平方公里范围的稀土矿含钪70t,经济价值超700亿元.稀土是国家战略储备资源,这次发现的钪更能被用在国防、军工、航天、核能等多个重要方面.
(5)、对1-18号元素的原子结构示意图进行分析,可以发现许多规律,如在同一周期,从左到右,核外电子数依次递增。请再总结出其它规律,并写出其中一条:。35. 资料一:据报道,浙西北藏着个聚宝盆,4平方公里范围的稀土矿含钪70t,经济价值超700亿元.稀土是国家战略储备资源,这次发现的钪更能被用在国防、军工、航天、核能等多个重要方面.资料二:根据“嫦娥一号”从月球返回的信息表明,月球中含有丰富He﹣3原子,同时测了月球上14种元素的含量和分布:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn(锰)、Cr(铬)、Gd(钆).请结合上述材料回答:
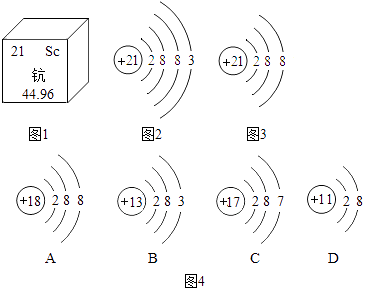 (1)、“嫦娥一号”从月球返回信息表明,月球中含有丰富He﹣3原子,它可能成为未来核能的重要原料.He﹣3原子核内A、含有3个质子,没有中子 B、含有2个质子,1个中子 C、含有1个质子,2个中子 D、含有3个中子,没有质子(2)、钪元素相关信息如图1所示.下列说法中不正确的是 .A、该元素的元素符号为Sc B、该元素属于金属元素 C、该元素的原子核外有21个电子 D、该元素的相对原子质量为44.96g(3)、“嫦娥一号”另一个目标是探测下列14种元素的含量和分布:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn(锰)、Cr(铬)、Gd(钆).其中属于地壳中含量最多金属是;属于非金属元素的有种.(4)、钪是一种熔点高、密度小、抗腐蚀性能好的金属.钪(Sc)元素的粒子结构示意图如图2所示:
(1)、“嫦娥一号”从月球返回信息表明,月球中含有丰富He﹣3原子,它可能成为未来核能的重要原料.He﹣3原子核内A、含有3个质子,没有中子 B、含有2个质子,1个中子 C、含有1个质子,2个中子 D、含有3个中子,没有质子(2)、钪元素相关信息如图1所示.下列说法中不正确的是 .A、该元素的元素符号为Sc B、该元素属于金属元素 C、该元素的原子核外有21个电子 D、该元素的相对原子质量为44.96g(3)、“嫦娥一号”另一个目标是探测下列14种元素的含量和分布:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn(锰)、Cr(铬)、Gd(钆).其中属于地壳中含量最多金属是;属于非金属元素的有种.(4)、钪是一种熔点高、密度小、抗腐蚀性能好的金属.钪(Sc)元素的粒子结构示意图如图2所示:①如图4四种粒子的结构示意图中,与图1化学性质相似的是 .
②图3所表示的粒子的化学符号是 .
四、实验探究题
-
36. 如下图所示,将滴有酚酞的滤纸条放在试管里,试管口塞上一团脱脂棉 :酚酞遇氨水变红色
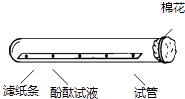 (1)、用仪器A吸取浓氨水,加在试管口的棉花上 滴 ,A的名称是 .(2)、实验中,观察到的现象是 ,这说明 .(3)、如果在实验中发现试管里滤纸条没有变色,而试管口所塞的棉花却变成了红色,导致这种现象产生错误操作可能是37. 某兴趣小组做如下实验探究微粒的运动.请回答实验中的有关问题.
(1)、用仪器A吸取浓氨水,加在试管口的棉花上 滴 ,A的名称是 .(2)、实验中,观察到的现象是 ,这说明 .(3)、如果在实验中发现试管里滤纸条没有变色,而试管口所塞的棉花却变成了红色,导致这种现象产生错误操作可能是37. 某兴趣小组做如下实验探究微粒的运动.请回答实验中的有关问题.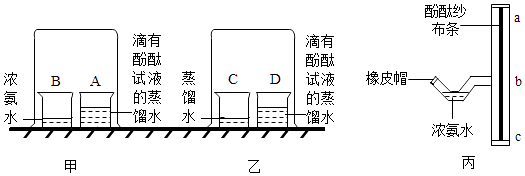 (1)、实验I:在盛有少量蒸馏水的小烧杯中滴入2~3滴酚酞试液,再向其中滴加浓氨水,由实验I得出的结论有 .(2)、实验Ⅱ(如图甲所示):烧杯B中的现象是;产生这一现象的原因是 .(3)、为使实验结论准确可靠,该兴趣小组设计实验Ⅲ(如图乙所示)作为对比实验.你认为有无必要(填“有”或“无”),理由是 .(4)、【发现问题】虽然课本上这个实验的现象明显,但也存在一些不足,如:氨水的用量大、实验装置无法固定、有很多氨气逸出大烧杯等.
(1)、实验I:在盛有少量蒸馏水的小烧杯中滴入2~3滴酚酞试液,再向其中滴加浓氨水,由实验I得出的结论有 .(2)、实验Ⅱ(如图甲所示):烧杯B中的现象是;产生这一现象的原因是 .(3)、为使实验结论准确可靠,该兴趣小组设计实验Ⅲ(如图乙所示)作为对比实验.你认为有无必要(填“有”或“无”),理由是 .(4)、【发现问题】虽然课本上这个实验的现象明显,但也存在一些不足,如:氨水的用量大、实验装置无法固定、有很多氨气逸出大烧杯等.【查阅资料】
①氨气的密度比空气的密度小.
②T形三通管属于微型化学仪器.
【实验改进】在老师指导下,同学们改用图丙装置探究微粒的运动性.
在T形三通管的粗玻璃管里,固定一根湿润的酚酞纱布条.
用(填写仪器名称)吸取少许浓氨水,将其滴入T形三通管的细弯管处,然后用橡皮帽封闭管口.
(5)、一会儿,观察到(填“ba”或“bc”)段纱布条变成红色.(6)、微热细弯管处的浓氨水,纱布条变红的速率会加快.【实验反思】改进实验与课本实验相比较,有不少的优点,请你写出其中的一条 .
38. 小英同学在距一支粉笔的粗端2cm处点上一滴蓝墨水,将粉笔插入盛有酒精的培养皿中.过了一段时间发现随着酒精的上升,蓝墨水在粉笔上不断移动,最后蓝墨水在粉笔上形成两个比较明显的区域(如图所示).试根据上述现象回答问题: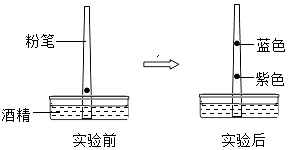 (1)、蓝墨水属于(填“纯净物”或“混合物”).(2)、由此实验可以作出的推测是(填序号)
(1)、蓝墨水属于(填“纯净物”或“混合物”).(2)、由此实验可以作出的推测是(填序号)①用滤纸代替粉笔重复上述实验,也能得到相似的实验现象;
②不同分子在同种介质(如粉笔)中运动速度不同;
③粉笔和酒精一定会发生化学反应
(3)、上述实验还可以说明分子在运动.请举一例说明分子之间有间隔 .39. 课堂上老师按图I装置进行分子运动实验时同学们闻到了一股难闻的刺激性气味,课后在老师的指导下,同学们对原实验装置进行了改进,装置如图II所示.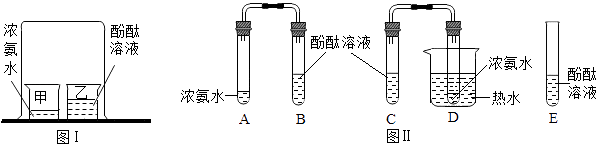 (1)、图I大烧杯中的实验现象是(填“甲”或“乙”)小烧杯中溶液变成了红色.(2)、同学们按图II装置进行了如下实验操作.
(1)、图I大烧杯中的实验现象是(填“甲”或“乙”)小烧杯中溶液变成了红色.(2)、同学们按图II装置进行了如下实验操作.【步骤1】向B、C、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色.
【步骤2】在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中.
回答问题:
①实验中,E所起的作用是 .
②由此实验可以得出分子运动速率与有关.除此之外,改进后的实验还具有的优点是
(填序号).
A.可证明分子间有间隔 B.可证明分子的质量和体积都很小
C.环保,对环境污染小 D.可验证氨分子能使酚酞溶液变红.
40. 为了探究分子的运动性,小强进行下面的实验:步骤一:如图1所示:
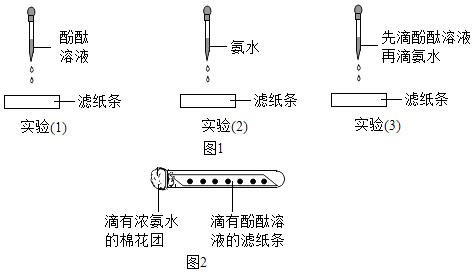 (1)、实验(3)中,滤纸条的变化情况是: .(2)、分析上面三个实验的现象,简单解释滤纸变红的原因? .
(1)、实验(3)中,滤纸条的变化情况是: .(2)、分析上面三个实验的现象,简单解释滤纸变红的原因? .步骤二:小强用剪刀在滤纸上剪取一条长滤纸,并在滤纸条上间隔地滴入酚酞溶液,然后放进试管里.最后用蘸有浓氨水的棉花团塞住试管(如图2所示)观察现象.
(3)、上面实验观察到的现象是 , 说明分子 .该实验还说明浓氨水的物理性有 . 步骤一在整个探究实验中所起的作用是 .
五、计算题