广西平南县2016-2017学年九年级初中毕业班化学第一次教学质量监测考试试卷
试卷日期:2017-11-10 考试类型:中考模拟
一、选择题
-
1. 化学实验操作的正确性、规范性是科学探究成败的关键因素之一.下列实验操作中,错误的是( )A、熄灭酒精灯火焰
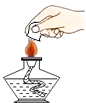 B、氧气验满
B、氧气验满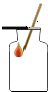 C、检查装置的气密性
C、检查装置的气密性 D、蒸发食盐水
D、蒸发食盐水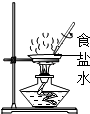 2. 夏季汽车轮胎容易发生爆炸,这是因为轮胎内的气体分子( )A、体积增大 B、质量增大 C、间隔增大 D、个数增多3. 下列材料中,属于有机合成材料的是( )A、蚕丝 B、羊毛 C、涤纶 D、棉花4. 打雷放电时,空气中有极少量氧气会转化成臭氧O3 , 下列有关说法中正确的是( )A、该变化是物理变化 B、O2是O3都是单质 C、O2与O3是相同的物质 D、O2与O3的性质完全相同5. 对于天宫一号目标飞行器内镍氢电池的总反应式H2+2NiO(OH)═2Ni(OH)2 , 下列叙述不正确的是( )A、H2是单质 B、NiO(OH)是氧化物 C、Ni(OH)2中Ni化合价为+2价 D、参加反应的H2、NiO(OH)的质量比为1:926. 等质量的碳素钢、生铁放入两支试管中各加入过量的稀盐酸,充分反应后产生氢气的情况是( )
2. 夏季汽车轮胎容易发生爆炸,这是因为轮胎内的气体分子( )A、体积增大 B、质量增大 C、间隔增大 D、个数增多3. 下列材料中,属于有机合成材料的是( )A、蚕丝 B、羊毛 C、涤纶 D、棉花4. 打雷放电时,空气中有极少量氧气会转化成臭氧O3 , 下列有关说法中正确的是( )A、该变化是物理变化 B、O2是O3都是单质 C、O2与O3是相同的物质 D、O2与O3的性质完全相同5. 对于天宫一号目标飞行器内镍氢电池的总反应式H2+2NiO(OH)═2Ni(OH)2 , 下列叙述不正确的是( )A、H2是单质 B、NiO(OH)是氧化物 C、Ni(OH)2中Ni化合价为+2价 D、参加反应的H2、NiO(OH)的质量比为1:926. 等质量的碳素钢、生铁放入两支试管中各加入过量的稀盐酸,充分反应后产生氢气的情况是( )
A、一样多 B、钢产生得多 C、生铁产生得多 D、无法比较7. 要除去下列物质中的少量杂质(括号内物质为杂质),下列实验方案设计中,不合理的是( )A、NaCl溶液(Na2SO4):加入过量的BaCl2溶液,过滤 B、N2 (O2):将气体缓缓通过灼热的铜网 C、CaCO2 (CaCl2):加水溶解一过滤一洗涤一干燥 D、KCl溶液(K2CO3):加入适量的稀盐酸8. 已知 表示氢原子质子数为1,相对原子质量为2,则
表示氢原子质子数为1,相对原子质量为2,则 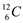 和
和  中不同的是( )。 A、质子数 B、电子数 C、相对原子质量 D、中子数9. 下列有关物质的变化中属于化学变化的是( )A、木材制成桌椅 B、食物腐烂 C、蔗糖熔化 D、冬天窗花形成10. 下列的各物质属于纯净物的是( )
中不同的是( )。 A、质子数 B、电子数 C、相对原子质量 D、中子数9. 下列有关物质的变化中属于化学变化的是( )A、木材制成桌椅 B、食物腐烂 C、蔗糖熔化 D、冬天窗花形成10. 下列的各物质属于纯净物的是( )
A、氢气在氧气中燃烧所得的液体 B、碘酒 C、合金 D、稀硫酸11. 下列说法错误的是( )
A、基本营养素包括蛋白质、糖类、油脂、维生素、无机盐和水六大类 B、为防止骨质疏松,应多食用奶制品、豆类、虾皮等食物 C、回收废弃塑料不仅减少白色污染,而且节约资源 D、食品添加剂是用于改善食物品质、口感的可食用物质,添加越多越好12. 某钠盐溶液中含有Cl﹣、OH﹣、CO32﹣三种阴离子,仅用一份样品溶液,利用下面的试剂与操作就可将溶液中的三种阴离子依次检验出来,正确的实验操作顺序是( )①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液。
A、①②④②③ B、③②①②④ C、④②①②③ D、④②③②①13. 有一种生活中常见的燃料,现在取这种燃料2.3g在足量氧气中充分燃烧,生成4.4g二氧化碳和2.7g水,则你认为该燃料可能是( )
A、C2H5OH B、C2H4 C、CH4 D、C2H614. a、b、c三种酸分别与足量的金属Mg充分反应,生成等质量的H2 , 反应消耗a、b、c的分子数目之比为3:6:2.下列关于a、b、c的推理合理的是(HX、H2Y、H3Z分别表示三种酸)( )A、a、b、c可能分别为HX、H3Z 、H2Y B、a、b、c可能分别为H2Y、H3Z 、HX C、a、b、c可能分别为HX 、H2Y、H3Z D、a、b、c可能分别为H2Y、HX 、H3Z15. 下列图象一定不能正确反映其对应关系的是( )A、某温度下,向一定量的氯化钠溶液中不断加入水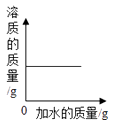 B、向一定量的氢氧化钠和氯化钠的混合溶液中逐滴加入氯化铁溶液
B、向一定量的氢氧化钠和氯化钠的混合溶液中逐滴加入氯化铁溶液 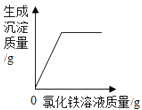 C、向一定量的氢氧化钠溶液中逐滴加水稀释
C、向一定量的氢氧化钠溶液中逐滴加水稀释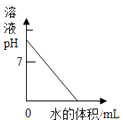 D、向两个分别盛有质量相等的氢氧化镁和氧化镁固体的烧杯中,逐滴加入溶质质量分数相同的稀盐酸
D、向两个分别盛有质量相等的氢氧化镁和氧化镁固体的烧杯中,逐滴加入溶质质量分数相同的稀盐酸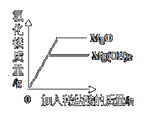
二、填空题
-
16. 请用数字和化学符号填空:
(1)、2个铅原子;(2)、两个硝酸根离子;(3)、人体中含量最多的金属元素;(4)、保持干冰化学性质的最小粒子是。
17. 近年来,如图的情况仍有发生,令人痛心,请你分析发生这种事故的主要原因是。产生这种无形杀手的物质主要是 (写化学式),常温下,它是一种色味的气体。
为了避免类似事故发生应如何改进。
 18. 向AgNO3、Cu(NO3)2、Mg(NO3)2混合液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,无气体生成,则滤出的固体中一定含有 , 滤液中一定含有的阳离子是。
18. 向AgNO3、Cu(NO3)2、Mg(NO3)2混合液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,无气体生成,则滤出的固体中一定含有 , 滤液中一定含有的阳离子是。
19. 如图是A,B,C三种固体物质的溶解度曲线.请回答下列问题: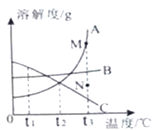 (1)、t1℃时,三种物质的溶解度大小顺序为。(2)、当A中混有少量B时,可用 方法提纯A。(3)、将A,B,C的饱和溶液从t3℃降温到t2℃,的溶液中无晶体析出。(4)、若要将N点的A溶液转变为M点的A溶液,可采用的方法。20. 为改善食品的营养和味道,在食品制作过程中常用到食品添加剂。(1)、食品添加剂的使用应严格遵照国家标准。稳定态二氧化氯作为蔬菜防腐剂的最大使用量为0.01g/kg,ClO2中Cl元素的化合价为。(2)、为打击在食品中滥用添加剂的行为,卫生部公布了47种“违法添加的非食用物质”名单,孔雀石绿(化学式C23H25ClN2)是其中的一种。关于孔雀石绿下列说法不正确是(填序号)。
(1)、t1℃时,三种物质的溶解度大小顺序为。(2)、当A中混有少量B时,可用 方法提纯A。(3)、将A,B,C的饱和溶液从t3℃降温到t2℃,的溶液中无晶体析出。(4)、若要将N点的A溶液转变为M点的A溶液,可采用的方法。20. 为改善食品的营养和味道,在食品制作过程中常用到食品添加剂。(1)、食品添加剂的使用应严格遵照国家标准。稳定态二氧化氯作为蔬菜防腐剂的最大使用量为0.01g/kg,ClO2中Cl元素的化合价为。(2)、为打击在食品中滥用添加剂的行为,卫生部公布了47种“违法添加的非食用物质”名单,孔雀石绿(化学式C23H25ClN2)是其中的一种。关于孔雀石绿下列说法不正确是(填序号)。A.孔雀石绿属于有机物 B.孔雀石绿由C,H,Cl、N四种原子构成
C.孔雀石绿中H元素的质量分数最大 D.孔雀石绿不能食用
(3)、小刚在实验室发现了一块绿色的孔雀石标本,想知道绿孔雀石和孔雀石绿的化学成分是否相同,和课外小组的同学一起探究,实验流程如图: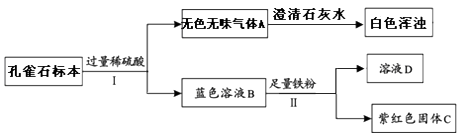
①小刚依据上述实验得出结论:孔雀石绿和绿色的孔雀石并非同种物质,绿色孔雀石中一定含有的元素有(写元素符号)。
②实验Ⅱ中发生反应的化学方程式。
21. 下列物质均为初中化学中常见的物质,其中A、B的组成元素相同,A、B、D、E、F为氧化物,H为改良酸性土壤常用的物质,下图是它们之间的转化关系,请回答: (1)、写出下列物质的化学式:H _;(2)、若J为蓝色沉淀,写出I和G反应生成J的化学方程式。
(1)、写出下列物质的化学式:H _;(2)、若J为蓝色沉淀,写出I和G反应生成J的化学方程式。三、实验探究题
-
22. 如图所示为实验室中常见气体设备、净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学欲利用其进行下列各探究实验.
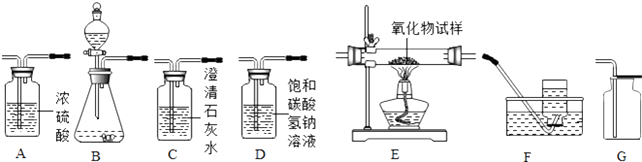 (1)、以石灰石和稀盐酸为原料,在实验室中制备并收集干燥、纯净的二氧化碳气体,按照要求设计实验装置、连接仪器,并检验装置的气密性.
(1)、以石灰石和稀盐酸为原料,在实验室中制备并收集干燥、纯净的二氧化碳气体,按照要求设计实验装置、连接仪器,并检验装置的气密性.①所选仪器的连接顺序为(从左到右填写仪器序号字母)(提示:挥发出少量HCl气体可用饱和碳酸氢钠溶液吸收)。
②用石灰石和稀盐酸制取二氧化碳的化学方程式为。
③若将二氧化碳气体通入酚酞试液中,试液显色。
(2)、用一氧化碳气体(含少量水蒸气)测定某铁的氧化物(Fe2O3)的元素组成比例,并验证反应中气体生成物的性质,所选仪器按A1→E→C→A2顺序连接按(A1、A2为浓硫酸洗气瓶),并检验装置的气密性,所设计的实验装置中气体流向是从左向右.①反应前大玻璃管中加入铁的粉末状氧化物(FexOy)试样的质量为16 g,实验结束后,继续通入一氧化碳气体,直至大玻璃管冷却.这时测量到E处大玻璃管中粉末状固体的质量减少了4.8 g,试推算该铁的氧化物的化学式中x、y的比值: . (设所发生的反应均完全进行)
②将少量二氧化碳通入大量澄清石灰水中,出现白色浑浊,且溶液质量减少.试解释溶液质量减小的原因:。
③对于该实验方案设计还存在不完善之处,你的具体改进方案是。
23. 不锈钢材料中含有的金属铬(Cr)能提高钢的抗氧化性和耐腐蚀性.为了解金属铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,小娟与小涛进行了如下探究活动.(1)、【猜想和假设】根据所学知识,猜想三种金属在金属活动顺序中的相对位置关系:猜想一:Cr Al Cu 猜想二:Al Cr Cu 猜想三:。
(2)、【实验和探究】小娟的实验:取大小相同的铝、铬、铜三种金属片(用砂纸打磨光亮)
实验步骤
实验现象
解释与结论
分别取三支试管,向其中入等质量、等浓度的稀硫酸,然后将铝、铬、铜三种金属分别插入三支试管中.
铝片表面产生的气泡较快;
铬片表面产生气泡较缓慢,溶液变蓝色;
铜片无明显现象.
猜想成立.
铬与稀硫酸反应生成蓝色的
硫酸亚铬(CrSO4)溶液,该反应的化学方程式为 .
(3)、小涛的实验:小涛只选用了三种药品进行实验,也得出了三种金属在金属活动顺序中的相对位置关系.则他选用的三种药品可能是 .
【总结与归纳】由上述实验得出比较金属活动性强弱的方法有:①_②_。
四、计算题
-
24. 菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示:
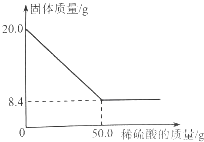
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O ②菱铁矿中杂质不参加反应,且难溶于水.
请计算:
(1)、20.0g菱铁矿中FeCO3的质量为g。(2)、列式计算所用稀硫酸的溶质质量分数(结果准确到0.1%)。