2016年广西钦州市中考化学试题
试卷日期:2017-11-07 考试类型:中考真卷
一、选择题
-
1. 下列仪器中,其名称为烧杯的是( )
A、 B、
B、 C、
C、 D、
D、 2. 下列气体中,能供给动植物呼吸的是( )
2. 下列气体中,能供给动植物呼吸的是( )
A、氮气 B、氧气 C、二氧化碳 D、稀有气体3. 下列物质中,硬度最大的是( )
A、石墨 B、木炭 C、金刚石 D、活性炭4. 下列属于无机非金属材料的是( )A、陶瓷 B、不锈钢 C、塑料 D、橡胶5. 下列属于纯净物的是( )
A、空气 B、蒸馏水 C、海水 D、铝合金6. 下列做法中,不利于节约用水的是( )
A、用洗过衣服的水拖地板 B、用淘米水浇花 C、及时修理坏了的水龙头 D、漱口时不关闭水龙头7. 下列化学式的读法错误的是( )
A、SO2(二氧化硫) B、HNO3(硝酸) C、KCl(氯化钾) D、Na2SO4(硫氧化钠)8. 下列物质溶于水后,溶液温度降低的是( )
A、氯化钠 B、生石灰 C、硝酸铵 D、浓硫酸9. 用扇子扇灭蜡烛火焰的灭火原理是( )
A、隔绝空气 B、降低可燃物的着火点 C、清除可燃物 D、使温度降到可燃物的着火点以下10. 从分子的角度,右图所示说明了 ( ) A、分子是由原子构成的 B、分子在不断地运动 C、分子的质量和体积都很小 D、分子间存在间隔11. 硝酸钾的溶解度随温度升高而增大,将一杯室温下恰好饱和的硝酸钾溶液变为不饱和溶液,应选择( )A、加水 B、降温 C、取出部分溶液 D、恒温下加溶质12. 中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝.已知一种原子的中子数为173,下列关于该原子的说法错误的是( )A、质子数为116 B、核电荷数为116 C、核外电子数为173 D、相对原子质量为28913. 下列有关实验现象描述错误的是( )A、红磷在空气中燃烧,产生大量的白烟 B、木炭在氧气中燃烧,伴有蓝色火焰 C、一氧化碳在空气中燃烧,火焰呈浅蓝色 D、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体14. 某反应的微观示意图如下图所示,该反应属于( )
A、分子是由原子构成的 B、分子在不断地运动 C、分子的质量和体积都很小 D、分子间存在间隔11. 硝酸钾的溶解度随温度升高而增大,将一杯室温下恰好饱和的硝酸钾溶液变为不饱和溶液,应选择( )A、加水 B、降温 C、取出部分溶液 D、恒温下加溶质12. 中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝.已知一种原子的中子数为173,下列关于该原子的说法错误的是( )A、质子数为116 B、核电荷数为116 C、核外电子数为173 D、相对原子质量为28913. 下列有关实验现象描述错误的是( )A、红磷在空气中燃烧,产生大量的白烟 B、木炭在氧气中燃烧,伴有蓝色火焰 C、一氧化碳在空气中燃烧,火焰呈浅蓝色 D、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体14. 某反应的微观示意图如下图所示,该反应属于( )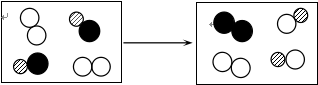 A、分解反应 B、化合反应 C、置换反应 D、复分解反应15. 下列事实能用金属活动性解释的是( )
A、分解反应 B、化合反应 C、置换反应 D、复分解反应15. 下列事实能用金属活动性解释的是( )
A、银的导电性比铝强 B、钨的熔点比铁高 C、黄铜的硬度比纯铜大 D、铁器比铜器容易生锈16. 下列实验方案设计不合理的是( )
A、用肥皂水鉴别硬水和软水 B、用稀盐酸除去铁粉中混有少量的铜粉 C、用pH试纸区别食盐溶液和纯碱溶液 D、用稀硝酸除去KNO3中混有的K2CO317. 在反应C + H2O CO + H2中,若生成物的总质量为15g,则参加反应的水的质量为( )
A、9g B、12g C、14g D、15g18. 右图是甲、乙两种固体物质的溶解度曲线。下列叙述正确的是( )
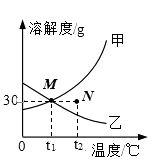
A、甲的溶解度大于乙的溶解度 B、t1℃时,甲、乙的饱和溶液溶质的质量分数均为30% C、t2℃时,N点表示甲物质的不饱和溶液 D、采用冷却结晶法从乙的饱和溶液中可得到晶体乙19. 下列各组内物质间的转化关系中,存在不能一步转化的是( )
A、Cu→CuO→CuSO4 B、H2O2→O2→P2O5 C、NaCl→NaNO3→NaOH D、Fe2O3→Fe→FeCl220. 下列各组内物质的溶液混合后,恰好完全反应,所得溶液的pH大于7的是( )
A、Na2CO3、HCl、NaOH B、BaCl2、H2SO4、Na2SO4 C、MgCl2、HNO3、AgNO3 D、Na2CO3、Ba(OH)2、KCl二、填空题
-
21. 用化学用语填空:
(1)、氮元素;(2)、两个钾离子;(3)、氧化钙;(4)、人体胃酸的主要成分;
(5)、氢氧化铜;
(6)、硫酸亚铁。
22. 中国本土科学家屠呦呦获得2015年诺贝尔生理学或医学奖,她的突出贡献是创制新型抗疟药——青蒿素和双氢青蒿素,挽救了全球特别是发展中国家的数百万人 的生命。回答:
(1)、青蒿素的化学式为C15H22O5 , 它属于(填“无机物”或“有机物”)。
(2)、利用乙醚提取青蒿素的主要流程是:干燥、破碎青蒿叶→在乙醚中浸泡、萃取→浓缩提取液→粗品→精制。其中“破碎青蒿叶”主要发生了变化。
(3)、医生用青蒿素给病人治疗的同时,让其多吃蔬菜,目的是补充病人体内所需营养素中的。(4)、青蒿中不仅含有青蒿素,还含有青蒿甲素(C15H22O3),它与青蒿素的组成元素(填“相同”或“不同”)。
23. 氢能是人们积极利用的新能源。根据下列装置回答: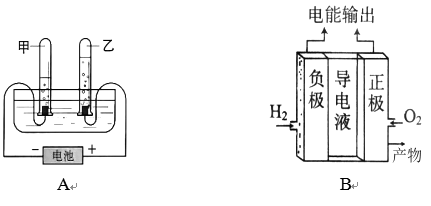 (1)、用A装置进行电解水实验,在甲试管内收集到的气体是。
(1)、用A装置进行电解水实验,在甲试管内收集到的气体是。
(2)、实验室制取氢气,可用以下药品中的(填序号)。①银和稀盐酸 ②锌和稀硫酸 ③氧化锌和稀盐酸
(3)、B装置是氢氧燃料电池,它把氢气和氧气反应的能直接转化为电能。这类电池已在宇宙飞船、太空站等航天器上使用,发电后的产物为 , 还可供宇航员饮用。
(4)、研究人员最新研发出CO2经过“烟囱”变燃料的技术:让CO2和H2混合后通过有镍纳米粒子的细铝管道,加热,在管道另一端出来的就是燃料。反应原理为:CO2 +4 H2 X +2H2O,其中X的化学式为 , 镍纳米粒子在反应中起作用。
X +2H2O,其中X的化学式为 , 镍纳米粒子在反应中起作用。
24. 结合下列图示的信息,回答: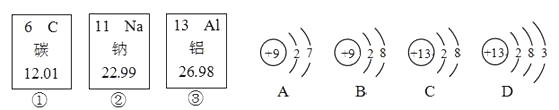 (1)、①、②、③中,属于非金属元素的是(填序号)。
(1)、①、②、③中,属于非金属元素的是(填序号)。
(2)、铝元素的相对原子质量为。
(3)、A,B,C,D中,容易失去电子的是(填字母,下同),属于阴离子的是。
(4)、②对应的碱与①的氧化物反应的化学方程式为。
25. 兴趣小组学习了单质、氧化物、酸、碱、盐的性质后进行了归纳,构建了下面的知识网络图。回答: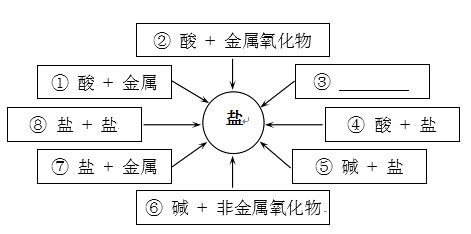 (1)、根据图示信息,③处的内容是。
(1)、根据图示信息,③处的内容是。
(2)、写出⑦中一个反应的化学方程式:。三、简答题
-
26. 完成实验报告的填写:
实验名称:铵态氮肥的检验。
实验目的:学习检验铵态氮肥的方法。
实验仪器和药品:研钵、试管、酒精灯、试管夹、胶头滴管、火柴、镊子、药匙、
氯化铵、碳酸氢铵、熟石灰、烧碱溶液、红色石蕊试纸、蒸馏水。
实验记录:
实验步骤
实验现象
实验结论、解释
⑴将氯化铵和熟石灰粉末在研钵中混合后,研磨,再闻气味。
闻到。
铵态氮肥与碱反应生成氨气。
⑵用碳酸氢铵进行类似(1)的实验。
⑶将烧碱溶液滴入装有氯化铵的试管中,稍稍加热,用湿润的接近试管口检验。
观察到。
氯化铵与烧碱反应的化学方程式为 , 氨水呈碱性。
⑷用碳酸氢铵进行类似(3)的实验。
27. 氯化钙在生活中常用作干燥剂、融雪剂。下图是某探究小组用含有MgCO3、MgSO4、Al2O3杂质的石灰石样品制取氯化钙的流程(所加入的试剂均为适量)。回答: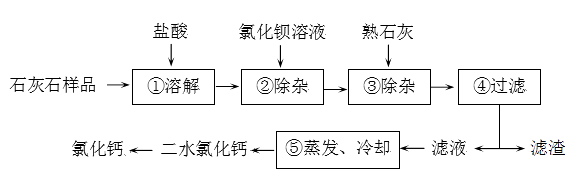 (1)、氯化钙中钙元素的化合价为。
(1)、氯化钙中钙元素的化合价为。
(2)、①中共发生了个化学反应。
(3)、②中除去的杂质离子是。
(4)、③中一个反应的化学方程式为。
(5)、滤渣的成分有氢氧化镁、和。
四、实验探究题
-
28. 规范操作是实验成功的前提。回答:(1)、实验用剩的药品(填“要”或“不要”)放回原瓶,(填“能”或“不能”)拿出实验室。
(2)、右图①、②操作中,正确的是(填序号)。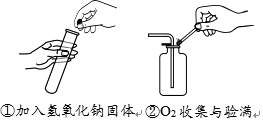
 (3)、不规范的操作会引起意外。在以下列举的四种意外中选择回答:
(3)、不规范的操作会引起意外。在以下列举的四种意外中选择回答:A.液体溅出伤人 B.着火引起意外 C.酒精溢出致火焰熄灭 D.试管骤冷破裂
操作③可能引起(填字母,下同);操作④可能引起。
29. 结合下列实验装置,回答: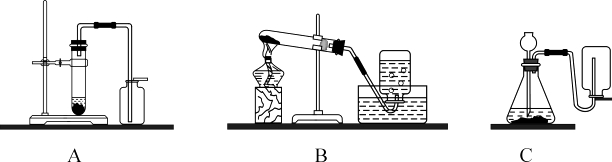 (1)、实验室若用分解暗紫色固体制取O2 , 该固体的名称是 , 可选(填字母,下同)装置。若用分解H2O2溶液制取O2 , 可选装置。
(1)、实验室若用分解暗紫色固体制取O2 , 该固体的名称是 , 可选(填字母,下同)装置。若用分解H2O2溶液制取O2 , 可选装置。
(2)、探究CO2性质的装置Ⅰ、Ⅱ如下:
①装置Ⅰ,将Y形导管平放于桌面上,通入CO2后,观察到a管中试纸变红色,b管中试纸无明显变化,此现象说明CO2能与反应,生成的使紫色石蕊变红色。
②装置Ⅱ,将Y形导管固定在铁架台上,a管在上方,b管在下方,通入CO2后,观察到b管中试纸先变红色且颜色较深,a管中试纸后变红色且颜色较浅,此现象说明CO2具有①所验证的性质外,还说明CO2的。
(3)、实验室制取CO2的化学方程式为 , 应选(填字母)装置,选择该装置的理由是。五、计算题
-
30. 我市沿海地区大量养殖贝类海产品,贝壳中含有的碳酸钙是重要的工业原料。为了测定某种贝壳中碳酸钙的含量,取贝壳样品25.0g放入烧杯中,分五次加入稀盐酸,每次充分反应后称量(杂质不与稀盐酸反应),所加入稀盐酸的质量与烧杯中物质的质量的关系如下表:
加入稀盐酸的总质量(g)
25.0
50.0
75.0
100.0
125.0
烧杯中物质的总质量(g)
47.8
70.6
93.4
116.2
141.2
计算:
(1)、当加入盐酸的总质量为50.0g时,充分反应后生成的气体质量是g。(2)、该贝壳样品中碳酸钙的质量分数。