2015年广西梧州市中考化学试卷
试卷日期:2017-11-03 考试类型:中考真卷
一、选择题
-
1. 不会造成空气污染的是( )A、一氧化碳 B、氧气 C、二氧化氮 D、可吸入颗粒物2. 下列气体因化学性质不活泼而常用作焊接金属的保护气的是( )A、氮气 B、水蒸气 C、二氧化碳 D、天然气3. 从下列图标中选出我国的“国家节水标志”( )A、
 B、
B、 C、
C、 D、
D、 4. 下列实验操作正确的是( )A、
4. 下列实验操作正确的是( )A、 读取液体体积
B、
读取液体体积
B、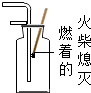 二氧化碳的验满
C、
二氧化碳的验满
C、 闻气体气味
D、
闻气体气味
D、 熄灭酒精灯
5. 下列说法不合理的是( )A、人体缺铁会引起贫血 B、青少年适量补钙,可以预防骨质疏松 C、人体缺碘会引起甲状腺肿大 D、霉变的花生可以用来榨油供人食用6. 下列属于化学变化的是( )A、铁水铸成锅 B、矿石粉碎 C、米饭变馊 D、二氧化碳气体变成干冰7. 下列物质能使紫色石蕊试液变红的是( )A、胃液 B、氨水 C、蔗糖水 D、pH约为7.8的鸡蛋清8. 下列物质属于有机物的是( )A、氦气 B、水 C、葡萄糖 D、焦炭9. 化学服务于生活,下列物质的用途错误的是( )A、用食醋除水垢 B、用工业用盐烹调海鲜 C、用盐酸除铁锈 D、建筑上用熟石灰与沙子混合来砌砖10. 湿的衣服经过晾晒会变干,这一现象说明( )A、分子之间有间隔 B、分子的质量很小 C、分子在不断运动 D、分子的体积很小11. 如图是两位同学对某一个化学方程式的描述,他们描述的化学方程式是( )
熄灭酒精灯
5. 下列说法不合理的是( )A、人体缺铁会引起贫血 B、青少年适量补钙,可以预防骨质疏松 C、人体缺碘会引起甲状腺肿大 D、霉变的花生可以用来榨油供人食用6. 下列属于化学变化的是( )A、铁水铸成锅 B、矿石粉碎 C、米饭变馊 D、二氧化碳气体变成干冰7. 下列物质能使紫色石蕊试液变红的是( )A、胃液 B、氨水 C、蔗糖水 D、pH约为7.8的鸡蛋清8. 下列物质属于有机物的是( )A、氦气 B、水 C、葡萄糖 D、焦炭9. 化学服务于生活,下列物质的用途错误的是( )A、用食醋除水垢 B、用工业用盐烹调海鲜 C、用盐酸除铁锈 D、建筑上用熟石灰与沙子混合来砌砖10. 湿的衣服经过晾晒会变干,这一现象说明( )A、分子之间有间隔 B、分子的质量很小 C、分子在不断运动 D、分子的体积很小11. 如图是两位同学对某一个化学方程式的描述,他们描述的化学方程式是( ) A、2H2O2=2H2O+O2↑ B、ZnO+2HNO3=Zn(NO3)2+H2O C、NH4Cl NH3↑+HCl↑ D、H2+CuO H2O+Cu12. 下列原子结构示意图所表示的原子,容易失去电子的是( )A、
A、2H2O2=2H2O+O2↑ B、ZnO+2HNO3=Zn(NO3)2+H2O C、NH4Cl NH3↑+HCl↑ D、H2+CuO H2O+Cu12. 下列原子结构示意图所表示的原子,容易失去电子的是( )A、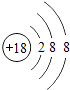 B、
B、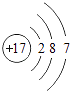 C、
C、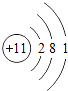 D、
D、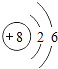 13. 配制一定溶质质量分数的氯化钠溶液,下列实验步骤中有错误的是( )A、计算:需要氯化钠、水的质量 B、称量:用托盘天平称量所需的氯化钠,放入烧杯中 C、量取:用量筒量取所需要的水,倒入装有氯化钠的烧杯中 D、溶解:振荡烧杯,使氯化钠溶解14. 今年清明期间,我市发生多起森林火灾,下列措施不能扑灭森林火灾的是( )A、高压水枪灭火 B、设法降低木材的着火点 C、直升飞机撒播灭火剂灭火 D、将大火蔓延路线前的树木砍掉,形成隔离带15. 下列有关酸、碱、盐的描述错误的是( )A、碳酸钠俗称烧碱 B、浓硫酸有强腐蚀性 C、氢氧化镁是一种碱 D、氯化钠溶液中,钠、氯元素均以离子形式存在16. 下列有关合金和金属的说法,错误的是( )A、铜可以与稀硫酸反应 B、合金的硬度一般比组成它们的纯金属更高 C、大多数金属为电的良导体 D、炼铁原理是利用一氧化碳与氧化铁反应生成铁17. 下列实验现象描述错误的是( )A、红磷燃烧产生大量白烟 B、点燃镁条发出耀眼的白光 C、生石灰与水反应放出热量 D、细铁丝在氧气中燃烧发出蓝色火焰18. 如图是化学变化的微观模拟图,“
13. 配制一定溶质质量分数的氯化钠溶液,下列实验步骤中有错误的是( )A、计算:需要氯化钠、水的质量 B、称量:用托盘天平称量所需的氯化钠,放入烧杯中 C、量取:用量筒量取所需要的水,倒入装有氯化钠的烧杯中 D、溶解:振荡烧杯,使氯化钠溶解14. 今年清明期间,我市发生多起森林火灾,下列措施不能扑灭森林火灾的是( )A、高压水枪灭火 B、设法降低木材的着火点 C、直升飞机撒播灭火剂灭火 D、将大火蔓延路线前的树木砍掉,形成隔离带15. 下列有关酸、碱、盐的描述错误的是( )A、碳酸钠俗称烧碱 B、浓硫酸有强腐蚀性 C、氢氧化镁是一种碱 D、氯化钠溶液中,钠、氯元素均以离子形式存在16. 下列有关合金和金属的说法,错误的是( )A、铜可以与稀硫酸反应 B、合金的硬度一般比组成它们的纯金属更高 C、大多数金属为电的良导体 D、炼铁原理是利用一氧化碳与氧化铁反应生成铁17. 下列实验现象描述错误的是( )A、红磷燃烧产生大量白烟 B、点燃镁条发出耀眼的白光 C、生石灰与水反应放出热量 D、细铁丝在氧气中燃烧发出蓝色火焰18. 如图是化学变化的微观模拟图,“ ”和“
”和“  ”表示不同元素的原子,下列说法正确的是( )
”表示不同元素的原子,下列说法正确的是( )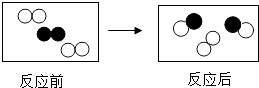 A、分子在化学变化中不可分 B、该反应是化合反应 C、原子在化学变化中可分 D、参加反应的两种物质分子个数比是2:119. 区分下列各组物质的方法可行的是( )A、用氯化铁溶液区分硫酸钾、硝酸钠两种溶液 B、用硝酸区分澄清石灰水和氢氧化钠稀溶液 C、常温下用水能区分一氧化碳和氮气 D、用盐酸能区分出碳酸氢铵、硫酸、硝酸银三种溶液20. 甲烷和一氧化碳的混合气体共4.4g,完全燃烧后生成二氧化碳气体8.8g,则混合气体中甲烷和一氧化碳的质量比为( )A、8:3 B、4:7 C、1:1 D、无法计算
A、分子在化学变化中不可分 B、该反应是化合反应 C、原子在化学变化中可分 D、参加反应的两种物质分子个数比是2:119. 区分下列各组物质的方法可行的是( )A、用氯化铁溶液区分硫酸钾、硝酸钠两种溶液 B、用硝酸区分澄清石灰水和氢氧化钠稀溶液 C、常温下用水能区分一氧化碳和氮气 D、用盐酸能区分出碳酸氢铵、硫酸、硝酸银三种溶液20. 甲烷和一氧化碳的混合气体共4.4g,完全燃烧后生成二氧化碳气体8.8g,则混合气体中甲烷和一氧化碳的质量比为( )A、8:3 B、4:7 C、1:1 D、无法计算二、填空题
-
21. 请用适当的化学符号或数字填空(化合价要标明“+”、“﹣”号).(1)、2个磷原子;(2)、氧化钠;(3)、NH3中氮元素化合价;(4)、镁离子 .22. 溶液和浊液在化学研究和实际生活中有重要作用.(1)、如图是Ca(OH)2溶解度曲线图,从图中分析,在30℃时,100g水中最多能溶解 g Ca(OH)2固体.30℃时,往装有Ca(OH)2饱和溶液的烧杯中加入少量Ca(OH)2固体,然后升温至40℃,所加入的Ca(OH)2固体(填“溶解”或“不溶解”).
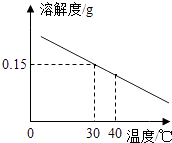 (2)、生活中常用石灰浆涂刷墙壁,一段时间后,墙壁表面变白变硬,请用化学方程式说明其原理: .(3)、生理盐水的溶剂是 .23. 人类每时每刻都离不开空气,没有空气就没有生机勃勃的地球.(1)、青藏高原空气稀薄,旅客易发生高原反应,出现呼吸困难的症状,他们常常会拿着一小瓶气体吸几下,以缓解症状.你认为瓶内气体的主要成分是 , 检验该气体最简单的方法是(2)、某地雨水水样的pH为5.9,该雨水酸雨(填“是”或“不是”),硫燃烧的生成物排入空气是造成酸雨的主要原因,硫燃烧的化学方程式为: .(3)、汽车尾气净化装置里装有金属钯(Pd),尾气在其表面发生反应转化为无害的气体,反应如下:2NO+2CO=2CO2+N2 . 金属钯(Pd)可使该反应更快进行,且Pd本身的质量和化学性质没有发生改变,则Pd在该反应中称作 .24. 请用学过的化学知识回答以下问题.(1)、物质的用途各不相同,请选择合适的化学式填空:
(2)、生活中常用石灰浆涂刷墙壁,一段时间后,墙壁表面变白变硬,请用化学方程式说明其原理: .(3)、生理盐水的溶剂是 .23. 人类每时每刻都离不开空气,没有空气就没有生机勃勃的地球.(1)、青藏高原空气稀薄,旅客易发生高原反应,出现呼吸困难的症状,他们常常会拿着一小瓶气体吸几下,以缓解症状.你认为瓶内气体的主要成分是 , 检验该气体最简单的方法是(2)、某地雨水水样的pH为5.9,该雨水酸雨(填“是”或“不是”),硫燃烧的生成物排入空气是造成酸雨的主要原因,硫燃烧的化学方程式为: .(3)、汽车尾气净化装置里装有金属钯(Pd),尾气在其表面发生反应转化为无害的气体,反应如下:2NO+2CO=2CO2+N2 . 金属钯(Pd)可使该反应更快进行,且Pd本身的质量和化学性质没有发生改变,则Pd在该反应中称作 .24. 请用学过的化学知识回答以下问题.(1)、物质的用途各不相同,请选择合适的化学式填空:NaCl、(C6H10O5)n、NaHCO3、NH4NO3、O3
①可用作化肥的是 , ②面粉的主要成分是 ,
③能吸收紫外线的是 .
(2)、分类法有助于我们对繁多的物质进行研究,请从下列物质中选择合适的填空:不锈钢、C60、四氧化三铁、KNO3溶液
①属于单质的是 , ②属于化合物的是 .
(3)、吸烟时放出的烟气中含有能与人体血红蛋白结合的物质是 .25. 水是宝贵的资源,我们都需要有保护水资源的意识.(1)、请你说出两个会导致水污染的因素: , .(2)、梧州的桂江清澈,西江浑浊,两江交汇处形成了著名景点﹣﹣鸳鸯江.小张同学用如图的简易净水装置处理一杯西江水,装置中纱布、小卵石、石英沙的作用是 , 活性炭的作用是 .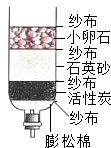 (3)、水中氢元素和氧元素的质量比 .
(3)、水中氢元素和氧元素的质量比 .三、简答题
-
26. 请回答下列问题.(1)、我市安装了很多太阳能路灯,很多家庭也用上了太阳能热水器,最近报道太阳能飞机正在进行环球飞行,这些都说明太阳能的应用前景无比广阔,请你说出太阳能作能源的两个优点.(2)、超市里卖的“84消毒液”有效成分是NaClO(次氯酸钠),可通过以下反应制取:Cl2+2X=NaClO+NaCl+H2O,则X的化学式是什么?你知道生活中还有什么物质可用来消毒?(任写一种)(3)、我市曾有传言:市面上的腐竹添加了塑料,理由是这些腐竹可以点燃且燃烧时产生黑烟.但仅凭这些就认定腐竹添加了塑料是不科学的.①已知腐竹的主要成分蛋白质是可燃的,请你用学过的化学知识解释:没有添加塑料的腐竹燃烧时也可能会产生黑烟.②塑料应用广泛,但随意丢弃会造成什么环境问题?27. A~H都是初中化学常见的物质,其中A含有钾元素,D是最常见的液体,E的溶液呈蓝色,F是蓝色的难溶物,G是白色的难溶物.它们之间的相互关系如图所示.请回答下面问题:
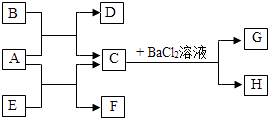 (1)、物质A的化学式: .(2)、物质E的化学式: .(3)、C与BaCl2溶液反应的化学方程式:(4)、F受热会发生分解反应,生成D和一种黑色固体,请写出该反应的化学方程式: .
(1)、物质A的化学式: .(2)、物质E的化学式: .(3)、C与BaCl2溶液反应的化学方程式:(4)、F受热会发生分解反应,生成D和一种黑色固体,请写出该反应的化学方程式: .四、实验题
-
28. 请根据下列图示,回答有关问题.
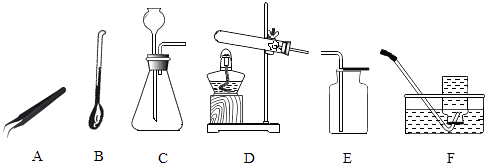 (1)、实验室用高锰酸钾制取氧气:取用高锰酸钾时应该选用(填字母序号),选用的发生装置是(填字母序号),反应的化学方程式为 .(2)、实验室制取氢气:选用的气体收集装置是(填字母序号),点燃氢气前必须 .29. 梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上标明锡纸的材质为“铝箔”.(1)、【提出问题】锡纸的材质到底是锡还是铝呢?小吴认为可以把锡纸放入盐酸中观察是否有气体放出来区别是锡还是铝,小周同学认为这样不能区别,理由是 .
(1)、实验室用高锰酸钾制取氧气:取用高锰酸钾时应该选用(填字母序号),选用的发生装置是(填字母序号),反应的化学方程式为 .(2)、实验室制取氢气:选用的气体收集装置是(填字母序号),点燃氢气前必须 .29. 梧州市某中学化学兴趣小组的同学到超市购买锡纸用于烧烤,同学们看见商品标签上标明锡纸的材质为“铝箔”.(1)、【提出问题】锡纸的材质到底是锡还是铝呢?小吴认为可以把锡纸放入盐酸中观察是否有气体放出来区别是锡还是铝,小周同学认为这样不能区别,理由是 .小施查阅资料发现锡的熔点为232℃,而铝的熔点为660℃,他用的方法区别出锡纸的材质是铝不是锡,接着同学们对铝这种金属进行了探究.
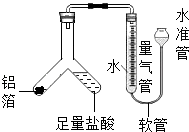
(2)、【探究活动一】铝的含量分析小施用如图装置测定铝箔中金属铝的含量,检验该装置气密性的操作是
(3)、若测得进入量气管的气体体积为100mL(氢气的密度为0.09g/L),铝箔中金属铝的质量为 g(铝箔中只有铝能与盐酸反应生成气体).(4)、【探究活动二】铝箔燃烧同学们做铝箔燃烧的实验.小吴用坩埚钳夹持一小块铝箔放在酒精灯火焰上,轻轻晃动,观察到铝箔熔化,失去了光泽,但铝箔并不燃烧;小周另取一块铝箔,用砂纸仔细打磨,再用坩埚钳夹持放在酒精灯火焰上,观察到铝箔仍不能燃烧.
小施同学认为铝箔不能在空气中燃烧是因为 , 这也是铝箔抗腐蚀性强的原因.
(5)、小施同学改进了实验,让铝箔燃烧并发出了耀眼的白光,小施同学的实验方案是 .(6)、【探究活动三】小吴将打磨后的铝片与铜盐溶液反应,现象如下:实验一:4mL 8% 的CuSO4溶液
实验二:4mL 8% 的CuCl2溶液
实验现象
短时间内无变化,一段时间后铝片上才出现少量红色的铜.
铝片上迅速有红色的铜出现.
①铝与氯化铜溶液反应的化学方程式为 .
②对比两个实验,小周推测对铝与铜盐溶液的反应可能有促进作用的离子是(填写离子符号),为了验证此推测,小施向实验一的CuSO4溶液中加入1g(填写化学式)固体,立即观察到铝片上出现大量红色的铜.
五、计算题
-
30. 取100g一定质量分数的Ba(OH)2溶液于烧杯中,逐渐加入质量分数为20%的H2SO4溶液.实验过程中,溶液的pH与加入H2SO4溶液的质量关系如图所示.
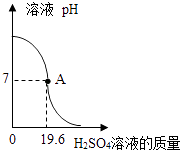 (1)、Ba(OH)2中钡元素的质量分数为 , 当加入9.8gH2SO4溶液时,溶液的pH(填“大于”“小于”或“等于”)7(2)、计算Ba(OH)2溶液中溶质的质量分数(写出计算过程)
(1)、Ba(OH)2中钡元素的质量分数为 , 当加入9.8gH2SO4溶液时,溶液的pH(填“大于”“小于”或“等于”)7(2)、计算Ba(OH)2溶液中溶质的质量分数(写出计算过程)