2013年广西贵港市中考化学试卷
试卷日期:2017-05-10 考试类型:中考真卷
一、我会选择
-
1. 下列物质的性质中,属于化学性质的是( )A、酒精易挥发 B、氯化钠易溶于水 C、石墨能导电 D、碳酸易分解2. 在空气中,氮气所占的体积分数大约是( )A、 B、 C、 D、3. 6000L氧气在加压的情况下可装入容积为40L的钢瓶中,是因为气体分子( )A、质量变小 B、间隔变小 C、体积变小 D、个数变少4. 下列物质在氧气中充分燃烧,能产生大量白烟的是( )A、硫 B、红磷 C、木炭 D、细铁丝5. 下列粒子结构示意图中,表示阴离子的是( )A、
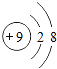 B、
B、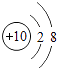 C、
C、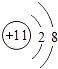 D、
D、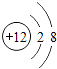 6. 下列有关水的认识中不正确的是( )A、自然界中的水都是混合物 B、过滤可使硬水软化 C、水是一种重要的溶剂 D、电解水时,负极上产生的气体是氢气7. C3N4是一种新型材料,它的硬度比金刚石还大,可用作切割工具.新型材料C3N4属于( )A、混合物 B、单质 C、氧化物 D、化合物8. 下列食物中富含糖类的是( )A、大米 B、鸡蛋 C、黄瓜 D、花生油9. 下列图示实验操作正确的是( )A、
6. 下列有关水的认识中不正确的是( )A、自然界中的水都是混合物 B、过滤可使硬水软化 C、水是一种重要的溶剂 D、电解水时,负极上产生的气体是氢气7. C3N4是一种新型材料,它的硬度比金刚石还大,可用作切割工具.新型材料C3N4属于( )A、混合物 B、单质 C、氧化物 D、化合物8. 下列食物中富含糖类的是( )A、大米 B、鸡蛋 C、黄瓜 D、花生油9. 下列图示实验操作正确的是( )A、 振荡试管
B、
振荡试管
B、 闻气体气味
C、
闻气体气味
C、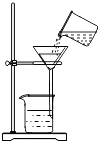 过滤
D、
过滤
D、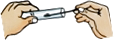 取用固体粉末
10. 下列说法不符合事实的是( )A、地壳中含量最高的金属元素是铁 B、在钢铁表面镀铬能防止钢铁生锈 C、多数合金的抗腐蚀性能比组成它们的纯金属更好 D、“真金不怕火炼”说明金的化学性质不活泼11. O2和Cl2都是活泼的非金属单质,在一定条件下它们都能跟甲烷反应,已知氧气和甲烷充分反应后的生成物是二氧化碳和水,由此推断氯气和甲烷充分反应后的生成物是( )A、C和HCl B、CH2Cl2和HCl C、CCl4和HCl D、CCl4和H212. 6月5日是“世界环境日”下列有关环境问题的叙述中不正确的是( )A、保护空气要减少有害气体和烟尘的排放 B、使用填埋法处理不能降解的生活垃圾 C、爱护水资源要节约用水和防止水体污染 D、努力实施“绿色化学”,把化学对环境的负面影响降到最低13. 有关物质的检验、鉴别、除杂,下列说法正确的是( )A、把燃着的木条伸入某集气瓶内,木条熄灭,说明瓶内的气体是CO2 B、用点燃的方法除去CO2中少有的CO C、不用另加试剂就可以把MgSO4、KOH、HCl、BaCl2四种溶液鉴别出来 D、向某溶液中加入BaCl2溶液,产生白色沉淀,过滤后沉淀中加入足量的稀硝酸,沉淀部分溶解并产生气泡,说明溶液中可能含有硫酸根离子14. 如表所列各组物质中,符合图示甲、乙、丙两两混合后发生反应的实验现象的是
取用固体粉末
10. 下列说法不符合事实的是( )A、地壳中含量最高的金属元素是铁 B、在钢铁表面镀铬能防止钢铁生锈 C、多数合金的抗腐蚀性能比组成它们的纯金属更好 D、“真金不怕火炼”说明金的化学性质不活泼11. O2和Cl2都是活泼的非金属单质,在一定条件下它们都能跟甲烷反应,已知氧气和甲烷充分反应后的生成物是二氧化碳和水,由此推断氯气和甲烷充分反应后的生成物是( )A、C和HCl B、CH2Cl2和HCl C、CCl4和HCl D、CCl4和H212. 6月5日是“世界环境日”下列有关环境问题的叙述中不正确的是( )A、保护空气要减少有害气体和烟尘的排放 B、使用填埋法处理不能降解的生活垃圾 C、爱护水资源要节约用水和防止水体污染 D、努力实施“绿色化学”,把化学对环境的负面影响降到最低13. 有关物质的检验、鉴别、除杂,下列说法正确的是( )A、把燃着的木条伸入某集气瓶内,木条熄灭,说明瓶内的气体是CO2 B、用点燃的方法除去CO2中少有的CO C、不用另加试剂就可以把MgSO4、KOH、HCl、BaCl2四种溶液鉴别出来 D、向某溶液中加入BaCl2溶液,产生白色沉淀,过滤后沉淀中加入足量的稀硝酸,沉淀部分溶解并产生气泡,说明溶液中可能含有硫酸根离子14. 如表所列各组物质中,符合图示甲、乙、丙两两混合后发生反应的实验现象的是甲
乙
丙
①
盐酸
Na2CO3溶液
Ca(OH)2溶液
②
盐酸
K2CO3溶液
CaCl2溶液
③
盐酸
K2CO3溶液
Ba(OH)2溶液
④
盐酸
Na2CO3溶液
BaCl2溶液
( )
 A、①② B、③④ C、①③ D、①②③④
A、①② B、③④ C、①③ D、①②③④二、我会填空
-
15. 请用数字和化学符号填空:(1)、碘元素;(2)、熔点最低的金属;(3)、2个亚铁离子;(4)、保持氨气化学性质的最小粒子 .16. 已知氯化钾(KCl)20℃时的溶解度是34g,50℃时的溶解度是42.6g.通过如图的实验操作得到相应的溶液①~⑤.
20℃时100g水中 ① ② ③ ④ ⑤
(1)、所得溶液中;为不饱和溶液的是(填序号,下同);溶质的质量分数相等的是;溶质的质量分数最大的是 .(2)、溶液④的质量为;该实验中把不饱和溶液转化为饱和溶液的方法是 .17. 化学与生活密切相关.请用相关的化学知识回答下列问题:(1)、如图是探究燃烧条件的实验,图中出现火焰的地方是点(填“a”、“b”、“c”)烧杯中热水的作用是升温和 .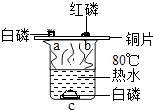 (2)、我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有作用.(3)、牛奶中含有丰富的能促进人体骨骼生长的主要元素,此元素是 .(4)、有机合成材料的出现是材料发展史上的一项重大突破,写出日常生活中一种常见的有机合成材料: .(5)、化肥对提高农作物的产量具有重要作用,仓库有一包久置失去标签的化肥,为了确认其成分,进行了如下实验:取样品,加入混合后研磨,产生刺激性气味的气体,说明该化肥为肥(填“氮”、“磷”、或“钾”)
(2)、我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有作用.(3)、牛奶中含有丰富的能促进人体骨骼生长的主要元素,此元素是 .(4)、有机合成材料的出现是材料发展史上的一项重大突破,写出日常生活中一种常见的有机合成材料: .(5)、化肥对提高农作物的产量具有重要作用,仓库有一包久置失去标签的化肥,为了确认其成分,进行了如下实验:取样品,加入混合后研磨,产生刺激性气味的气体,说明该化肥为肥(填“氮”、“磷”、或“钾”)三、我会回答
-
18. 根据相关内容填空:(1)、金属镓广泛用于制造半导体材料.镓的硫酸盐的化学式为Ga2(SO4)3 , 其中镓元素的化合价是价;(2)、肼(N2H4)具有很好的还原性,与氧反应的产物无污染,故可用于除去水中溶解的氧,以保护锅炉等设备.写出肼除氧时发生反应的化学方程式: , 该反应的基本反应类型是 .19. 某气体可能含有H2、CO、CO2和CH4四种气体中的一种或几种,为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每步都充分反应和吸收)
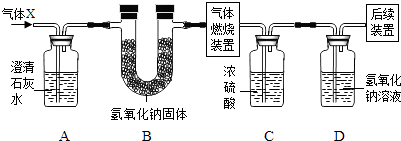
实验过程中装置A无明显变化;实验结束后装置C中增重5.4g,装置D中增重6.6g.
(1)、装置B在该实验中的作用是 .(2)、装置D中发生反应的化学方程式为 .(3)、该气体可能的组成有(填序号).①CH4②CH4和H2③CH4和CO2④CH4和CO ⑤H2和CO ⑥CH4、H2和CO
四、我会实验
-
20. 根据如图实验装置回答问题.
 (1)、写出图1中标有序号仪器的名称:①;② .(2)、选用装置B制氧气时发生反应的化学方程式为 .(3)、实验室制取二氧化碳所选用的收集装置为(填装置代号,下同).(4)、图2气体的发生装置中,在制二氧化碳时能起到“控制反应的发生或停止”效果的是 .21. 某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:CuSO4溶液分别与NaOH溶液、BaCl2溶液反应.实验结束后将两实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.(1)、写出废液混合后使滤液变无色时一定发生的反应的化学方程式: .(2)、取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液仍为紫色,则滤液呈性(填“酸”、“中”、“碱”).(3)、该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
(1)、写出图1中标有序号仪器的名称:①;② .(2)、选用装置B制氧气时发生反应的化学方程式为 .(3)、实验室制取二氧化碳所选用的收集装置为(填装置代号,下同).(4)、图2气体的发生装置中,在制二氧化碳时能起到“控制反应的发生或停止”效果的是 .21. 某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:CuSO4溶液分别与NaOH溶液、BaCl2溶液反应.实验结束后将两实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.(1)、写出废液混合后使滤液变无色时一定发生的反应的化学方程式: .(2)、取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液仍为紫色,则滤液呈性(填“酸”、“中”、“碱”).(3)、该小组的同学对滤液中溶质的成分继续进行了如下探究实验:【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想Ⅰ:;猜想Ⅱ;猜想Ⅲ .
(4)、【实验探究】实验操作
实验现象
实验结论
实验①:取少量滤液于试管中,加入适量的纯碱溶液,振荡.
无明显现象
猜想Ⅱ不成立
实验②
产生白色沉淀
猜想Ⅲ成立
在实验②的溶液中滴加无色酚酞溶液,观察到酚酞溶液变成红色.
【交流拓展】要使蓝色溶液变成无色,还可以用不同于上述原理的方法,即在蓝色溶液中加入足量的 .
五、我会计算
-
22. 用氢氧化钠溶液测定某硫酸溶液溶质的质量分数.实验如下:取25g该硫酸溶液,加入到烧杯中,然后把50g质量分数为10%的氢氧化钠溶液不断滴入烧杯中,同时用电子pH计不断读取反应时的pH,得出如图所示的关系,求;
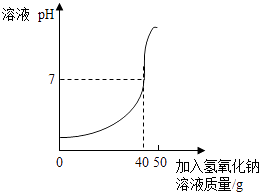 (1)、该硫酸溶液溶质的质量分数.(2)、配制500g上述硫酸溶液,所需质量分数为98%的硫酸溶液的质量.
(1)、该硫酸溶液溶质的质量分数.(2)、配制500g上述硫酸溶液,所需质量分数为98%的硫酸溶液的质量.